题目内容
有原子序数依次增大的五种短周期元素A、B、C、D、E,已知 A、E同主族,A在所有元素中原子结构最简单,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y;A、B、C、E四种元素都能与D元素分别形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是 ,E的原子结构示意图 。
(2)A与C形成化合物中含有的化学键属于(填“极性键”或“非极性键”) 。
(3)用电子式表示化合物E2D的形成过程 。
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式: 。
(10分)(1)第二周期ⅣA族(2分);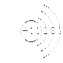 (2分)(2)极性键(2分)
(2分)(2)极性键(2分)
(3) (2分);(4)NH3 + H+=NH4+(2分)
(2分);(4)NH3 + H+=NH4+(2分)
解析试题分析:A在所有元素中原子结构最简单,则A应该是氢元素。B元素原子的最外层电子数是内层电子数的2倍,由于最外层电子数不能超过8个,所以B一定是第二周期因素,则B是碳元素。C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,因此C是氮元素,X是硝酸,Y是硝酸铵。A、B、C、E四种元素都能与D元素分别形成原子个数比不相同的常见化合物,这说明D应该是氧元素。A、E同主族,且E的原子序数最大,所以E是钠元素。
(1)碳元素的原子序数是6,在周期表中的位置是第二周期ⅣA族;Na的原子序数是11,其原子结构示意图是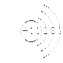 。
。
(2)A与C形成化合物是氨气,分子中含有的化学键属于极性键。
(3)氧化钠是含有离子键的离子化合物,其形成过程可表示为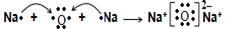 。
。
(4)氮元素的最高价氧化物的水化物与其氢化物反应的离子方程式NH3 + H+=NH4+。
考点:考查元素周期表第结构和元素周期律的应用以及常见化学用语的书写
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

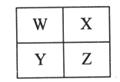
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强。
(1)Y在周期表中的位置是 。
(2)用电子式解释X与W能形成化合物X3W的原因 。
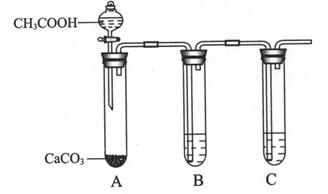
(3)X3W遇水可释放出使酚酞溶液变红的气体A,化学方程式是 。
(4)用惰性电极电解化合物XZ溶液从阴极释放出气体B,反应的离子方程式是 。
(5)已知W的单质与气体B在一定条件下可形成气体A,即: W2 (g)+3B (g)  2A(g) △H =-92.4 kJ?mol―1
2A(g) △H =-92.4 kJ?mol―1
在某温度时,一个容积固定的密闭容器中,发生上述反应。在不同时间测定的容器内各物质的浓度如下表:
| 时间 | 浓度(mol/L) | ||
| c(W2) | c(B) | c(A) | |
| 第0 min | 4.0 | 9.0 | 0 |
| 第10min | 3.8 | 8.4 | 0.4 |
| 第20min | 3.4 | 7.2 | 1.2 |
| 第30min | 3.4 | 7.2 | 1.2 |
| 第40min | 3.6 | 7.8 | 0.8 |
①W2的平均反应速率v(0min~10min)/ v(10min~20min) = ;
②反应在第10min改变了反应条件,改变的条件可能是 ;
a.更新了催化剂 b.升高温度 c.增大压强 d.增加B的浓度
③若反应从第30min末又发生了一次条件改变,改变的反应条件可能是 ;
a.更新了催化剂 b.升高温度 c.增大压强 d.减小A的浓度
三氟化氮是一种无色、无味、无毒且不可燃的气体、在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。NF3是一种三角锥形分子,键角102°,沸点-l29℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备NF3的化学反应方程式: 。
(2)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是 。
(3)与铜属于同一周期,且未成对电子数最多的元素基态原子核外电子排布式为 。
(4)理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是 ,配位数为 。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是 和 。
②T元素最可能是 (填“s”“P” “d”或“ds”等)区元素,位于 族。若T为第2周期元素,F是第3周期元素中原子半径最小的元素,则T与F形成化合物的空间构型为 ,其中心原子的杂化方式为 。
(13分)近现代战争中,制造坦克战车最常用的装甲材料是经过轧制和热处理后的合金钢,热处理后整个装甲结构的化学和机械特性和最大限度的保持一致。钢中合金元素的百分比含量为:铬0.5~1.25 镍0.5~1.5 钼0.3~0.6 锰0.8~1.6 碳0.3
(1)铬元素的基态原子的价电子层排布式是 。
(2)C元素与其同主族下一周期元素组成的晶体中,C原子的杂化方式为 .
(3)Mn和Fe的部分电离能数据如表:
| 元 素 | Mn | Fe | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
根据表数据,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
(4)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。
某镍配合物结构如右图所示,分子内含有的作用力
有 (填序号)。

A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是 。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是
(6)铁能与氮形成一种磁性材料,其晶胞结构如右图所示,则该磁性材料的化学式为