题目内容
【题目】己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:3![]() +8HNO3—→3
+8HNO3—→3![]() +8NO↑+7H2O
+8NO↑+7H2O

实验步骤如下:

Ⅰ.在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
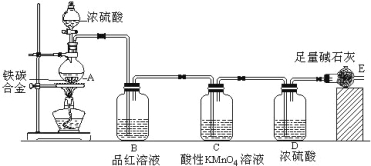
(1)装置b的名称为 ,使用时要从 (填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是
(2)本实验所用50%的硝酸的物质的量浓度为 ;实验中,氮氧化物废
气(主要成分为N02和NO)可以用NaOH溶液来吸收,其主要反应为:
2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20
其中NaOH溶液可以用Na2C03溶液来替代,请模仿上述反应,写出Na2C03溶液吸收的两个方程式:
;
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(4)为了除去可能的杂质和减少产品损失,可分别用 和 洗涤晶体。
【答案】(1)球形冷凝管(或冷凝管) 下口 平衡滴液漏斗与三颈烧瓶内的气压,使环己醇能够顺利流下
(2)10.4mol/L 2NO2+Na2CO3=NaNO2+NaNO3+CO2,NO2+NO+Na2CO3=2NaNO2+CO2
(3)将三颈烧瓶置于冷水浴中(“冰水浴”、“冰毛巾”、“减缓滴加速率”、“适当降低硝酸浓度”)
(4)苯
【解析】
试题分析:(1)由图像装置形状可知装置b的名称为球形冷凝管,为了确保冷凝效果,要从下口进冷水上口出,支管a作的是连通器,作用是平衡滴液漏斗与三颈烧瓶内的气压,使环己醇能够顺利流下。
(2)据公式:c=ρ![]() /M=1310×0.5/63=10.4mol/L,据已知反应2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20得Na2C03溶液吸收的两个方程式:2NO2+Na2CO3=NaNO2+NaNO3+CO2,NO2+NO+Na2CO3=2NaNO2+CO2。
/M=1310×0.5/63=10.4mol/L,据已知反应2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20得Na2C03溶液吸收的两个方程式:2NO2+Na2CO3=NaNO2+NaNO3+CO2,NO2+NO+Na2CO3=2NaNO2+CO2。
(3)要保证反应温度不致过高,一般用水浴加热。
(4)因为己二酸易溶于乙醇,不溶于苯,故可用苯除去可能的杂质和减少产品损失。

 阅读快车系列答案
阅读快车系列答案