题目内容
【题目】对于反应2A(g)+B(g)2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定: 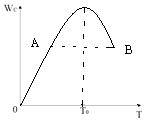
(1)T0对应的V正与V逆关系是V正V逆(填“>”、“<”、“=”).
(2)A、B两点正反应速率的大小关系VAVB(填“>”、“<”、“=”).
(3)温度T<T0时,Wc逐渐增大的原因是
(4)500℃条件下,该反应 K=2.33,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正)v(逆)(填“>”“<”或“=”)
【答案】
(1)=
(2)<
(3)反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多
(4)>
【解析】解:(1)由图可知,温度T0前,C的质量分数增大,故未达平衡,反应向正反应进行,温度T0后,C的质量分数减小,平衡向逆反应进行,故温度T0时,反应到达平衡状态,故V正=V逆 , 所以答案是:=(2)A、B两点,各组分的浓度相同,温度越高反应速率越快,故VA<VB ,
所以答案是:<;(3)温度T0前,反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多,
所以答案是:反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多;(4)测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则 ![]() =1<2.33,则平衡正向移动,正反应速率大于逆反应速率.
=1<2.33,则平衡正向移动,正反应速率大于逆反应速率.
所以答案是:>.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).

【题目】下表中物质的分类组合完全正确的是 ( )
编号 | A | B | C | D |
强电解质 | KNO3 | H2SO4 | BaSO4 | HNO3 |
弱电解质 | HF | CaCO3 | HClO | NH3 |
非电解质 | SO2 | CCl4 | H2O | C2H5OH |
A. A B. B C. C D. D