题目内容
【题目】氯化钠是日常生活的必需品,也是重要的化工原料。
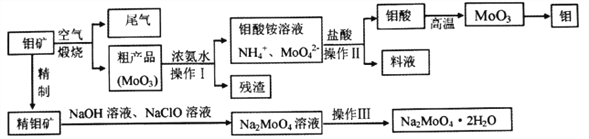
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。

提供的试剂:
Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、_____________、_____________;
②用离子方程式表示加盐酸的作用是________________;_______________________;
(2)实验所得纯NaCl的质量大于粗盐中NaCl的质量,原因是______________。
【答案】BaCl2 Na2CO3 H++OH—=H2O 2H++CO32—=H2O+CO2↑ 除去杂质的同时试剂之间反应,会发生反应生成NaCl
【解析】
(1)加入过量的氢氧化钠溶液可以除去氯化镁,加入过量的氯化钡溶液可以除去硫酸钠,加入过量的碳酸钠溶液可以除去氯化钙和过量的氯化钡;
(2)加入稀盐酸可以除去过量的氢氧化钠和过量的碳酸钠
(1)①依次滴加过量的氢氧化钠溶液、氯化钡溶液、碳酸钠溶液时,可以依次除去氯化镁、硫酸钠、氯化钙和过量的氯化钡;故填:BaCl2;Na2CO3。
②加入盐酸是为了中和氢氧化钠、与碳酸钠反应,从而把过量的氢氧化钠、碳酸钠除去,故填:H++OH-=H2O;2H++CO32—=H2O+CO2↑;
(2)除去杂质的同时试剂之间反应,会生成NaCl,,所以,纯NaCl的质量大于粗盐中NaCl的质量。
故填:除去杂质的同时试剂之间反应,会生成NaCl,。

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案【题目】已知反应A(g)+B(g) ![]() C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
温度/℃ | 700 | 830 | 1200 |
K值 | 1.7 | 1.0 | 0.4 |
A. 达到平衡后,B的转化率为50%
B. 增大压强,正、逆反应速率均加快
C. 该反应为吸热反应,升高温度,平衡正向移动
D. 反应初始至平衡,A的平均反应速率v(A)=0.005 mol·L-1·s-1