题目内容
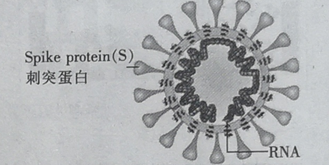
【题目】甲烷的分子结构模型如图所示:

根据甲烷的分子结构模型,回答问题:
(1)甲烷的电子式是__,其含义是__。
(2)甲烷的结构式是__,其含义是_。
(3)甲烷分子的空间构型是__。
(4)更能真实反映甲烷分子结构模型的是__。
【答案】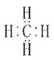 电子式可表示原子最外层电子成键情况
电子式可表示原子最外层电子成键情况  结构式除具有分子式表示的意义外,还能表示分子中原子的结合或排列顺序 正四面体结构 比例模型
结构式除具有分子式表示的意义外,还能表示分子中原子的结合或排列顺序 正四面体结构 比例模型
【解析】
本题考察了甲烷分子式、电子式、结构式表示的意义及其分子空间构型。电子式可表示原子最外层电子成键情况。结构式具有分子式所能表示的意义,能反映物质的结构,能表示分子中原子的结合或排列顺序,但不能表示其分子的空间构型。电子式可表示原子最外层电子成键情况。
(1)碳原子最外层有四个电子,和氢原子形成四对共用电子对,甲烷的电子式是 ,电子式可表示原子最外层电子成键情况;
,电子式可表示原子最外层电子成键情况;
故答案为: ;电子式可表示原子最外层电子成键情况;
;电子式可表示原子最外层电子成键情况;
(2)一对共用电子对表示一对共价键,所以甲烷的结构式是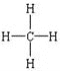 ,结构式具有分子式所能表示的意义,能反映物质的结构,能表示分子中原子的结合或排列顺序;
,结构式具有分子式所能表示的意义,能反映物质的结构,能表示分子中原子的结合或排列顺序;
故答案为: ;结构式除具有分子式表示的意义外,还能表示分子中原子的结合或排列顺序;
;结构式除具有分子式表示的意义外,还能表示分子中原子的结合或排列顺序;
(3)甲烷的价层电子对为四对,没有孤对电子,空间立体构型为正四面体形,甲烷分子为正四面体结构,碳原子位于正四面体中心,氢原子位于四个顶点上;
故答案为:正四面体结构;
(4)球棍模型和比例模型都能反映甲烷分子的空间构型,但比例模型更能形象的表达出氢原子、碳原子的位置及所占比例;
故答案为:比例模型。

 阅读快车系列答案
阅读快车系列答案【题目】已知:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
物质 | CH3OH | CH3OCH3 | H2O |
c/mol·L-1 | 0.08 | 1.6 | 1.6 |
A. 此时刻反应达到平衡状态
B. 容器内压强不变时,说明反应达平衡状态
C. 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率不变
D. 平衡时,反应混合物的总能量降低40 kJ
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
下列说法正确的是
A.ΔH1<0,ΔH2>0
B.反应①②③的反应热满足关系:ΔH1-ΔH2=ΔH3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取降温措施