题目内容
10.下列说法正确的是(NA表示阿伏加德罗常数的值)( )| A. | 常温常压下,18g NH4+所含的电子数为10NA | |
| B. | 56g金属铁与足量的稀盐酸反应时转移的电子数为3NA | |
| C. | 标准状况下,22.4L氧气所含的氧原子数为2 NA | |
| D. | 1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为4 NA |
分析 A.1个铵根离子含有10个电子;
B.铁与盐酸反应生成氯化亚铁;
C.体积转化为物质的量,结合1个氧气分子含有2个氧原子;
D.1mol过氧化钠和1mol氧化钠都含有2mol钠离子.
解答 解;A.常温常压下,18g NH4+的物质的量=$\frac{18g}{18g/mol}$=1mol,含的电子数为10NA,故A正确;
B.56g金属铁物质的量为1mol,与足量盐酸反应生成氯化亚铁,失去2mol电子,转移的电子数为2NA,故B错误;
C.标准状况下,22.4L氧气的物质的量为1mol,含有氧原子的物质的量为2mol,含的氧原子数为2 NA,故C正确;
D.1mol过氧化钠和1mol氧化钠都含有2mol钠离子,所以1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为2NA,故D错误;
故选:AC.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意过氧化钠的结构,题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 用含0.lmolFeCl3的溶液与足量沸水反应制得的Fe(0H)3胶体中胶粒数为0.1NA | |
| B. | 46g N02和N204的混合气体中含原子总数为NA | |
| C. | 标准状况下,5.6L CCl4含有的分子数为0.25NA | |
| D. | 0.25 mol Na2O2中含有的阴离子数为0.5 NA |
1.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH H2O | D. | NH3 H2O CO2 |
18.两种气态烃的混合物共0.1mol,充分燃烧后得3.58L(标准状况下)CO2和3.6g水,下列说法正确的是( )
| A. | 一定有甲烷 | B. | 一定有乙烯 | C. | 可能有乙烷 | D. | 无法计算 |
5.下列烷烃只有两种同分异构体的是( )
| A. | 丁烷 | B. | 丙烷 | C. | 乙烷 | D. | 戊烷 |
15.下列说法不正确的是( )
| A. | 含有较多钙、镁离子的水叫做硬水 | |
| B. | 热水瓶使用时间长了瓶胆内壁会产生一层水垢,其主要成分是CaCO3和MgCO3 | |
| C. | 硬水对生产生活带来许多不便,如在硬水中用肥皂洗涤衣物,不但难以洗净,还会使衣物变硬;煮硬水的锅炉要多用燃料,严重时可能造成锅炉爆炸等 | |
| D. | 生活中可以采用不同的方法将硬水软化,如煮沸法,磺化煤离子交换法等 |
2.表是某品牌柠檬汁饮料标签的部分内容,则该饮料中维生素C(分子式为C6H8O6)的物质的量浓度为( )
| Nutrition Facts营养成分 500mL含量 | |
| 热量 710kJ | 碳水化合物 42g |
| 蛋白质 0g | 脂肪酸 0g |
| 维生素C 100mg | |
| 中国居民膳食营养素日推荐摄入量(RNI):维生素C 100mg | |
| A. | 1.14×10-3 mol•L-1 | B. | 0.2 mg•mL-1 | ||
| C. | 1.42×10-3 mol•L-1 | D. | 0.2 mol•L-1 |
20.下列反应属于加成反应的是( )
| A. | CH4+Cl2→CH3 Cl+HCl | |
| B. | 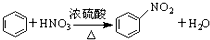 | |
| C. | 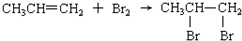 | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O |
