题目内容
某同学做“铝热反应”的实验.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3
熔点、沸点数据如下:
(1)铝热反应方程式为 .
(2)下列能与Al发生铝热反应的有 .(填序号)
A、MnO2 B、Na2O C、MgO D、FeO
(3)据上表数据该同学推测,铝热反应所得到的熔融物应是铁铝合金.若证明上述所得的块状熔融物中含有金属铝,所用试剂是 .
熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
(2)下列能与Al发生铝热反应的有
A、MnO2 B、Na2O C、MgO D、FeO
(3)据上表数据该同学推测,铝热反应所得到的熔融物应是铁铝合金.若证明上述所得的块状熔融物中含有金属铝,所用试剂是
考点:探究铝热反应
专题:金属概论与碱元素
分析:(1)铝和氧化铁在高温下发生反应生成氧化铝和铁,据此写出反应的化学方程式;
(2)铝热反应中制取的金属的还原性应该小于铝的还原性;
(3)铝可与氢氧化钠溶液反应,以此进行实验设计;
(2)铝热反应中制取的金属的还原性应该小于铝的还原性;
(3)铝可与氢氧化钠溶液反应,以此进行实验设计;
解答:
解:Ⅰ(1)铝和氧化铁在高温下发生反应生成氧化铝和铁,反应的化学方程式为:2Al+Fe2O3
2Fe+Al2O3,
故答案为:2Al+Fe2O3
2Fe+Al2O3;
(2)若铝热反应能够进行,制取的金属的还原性应该比金属铝还原性弱,选项中金属Na、Mg还原性强于Al,所以无法通过铝热反应制取,可用铝热法冶炼的金属为Mn和Fe,
故答案为:AD;
(3)铝可与氢氧化钠溶液反应,若证明上述所得的块状熔融物中含有金属铝,可加入氢氧化钠溶液进行检验,如果生成氢气,则说明含有铝,否则不含,
故答案为:氢氧化钠溶液.
| ||
故答案为:2Al+Fe2O3
| ||
(2)若铝热反应能够进行,制取的金属的还原性应该比金属铝还原性弱,选项中金属Na、Mg还原性强于Al,所以无法通过铝热反应制取,可用铝热法冶炼的金属为Mn和Fe,
故答案为:AD;
(3)铝可与氢氧化钠溶液反应,若证明上述所得的块状熔融物中含有金属铝,可加入氢氧化钠溶液进行检验,如果生成氢气,则说明含有铝,否则不含,
故答案为:氢氧化钠溶液.
点评:本题考查较为综合,涉及了铝热反应、金属铝检验、化学方程式书写等知识,试题侧重于学生的分析能力和实验能力的考查,注意相关实验原理、方法的把握,难度不大.

练习册系列答案
相关题目
下列实验中,溶液颜色有明显变化的是( )
| A、少量明矾溶液加入到过量NaOH溶液中 |
| B、往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C、少量Na2O2固体加入到过量NaHSO3溶液中 |
| D、往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A、若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| B、达到化学平衡时,4v正(O2)=5v逆(NO) |
| C、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D、化学反应速率关系是:v(正)>v(逆) |
砹(At)是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是( )
| A、砹易溶于某些有机溶剂 |
| B、砹化氢很不稳定易分解 |
| C、砹是有色气体 |
| D、砹化银不溶于水或稀HNO3 |
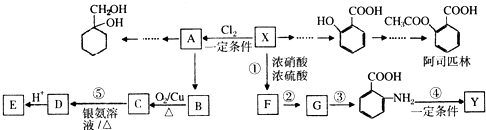
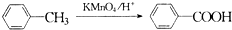
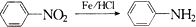 (苯胺,易被氧化)
(苯胺,易被氧化)
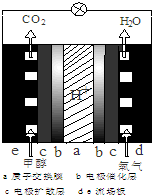 以甲醇为替代燃料是解决我国石油资源短缺的重要措施.
以甲醇为替代燃料是解决我国石油资源短缺的重要措施.