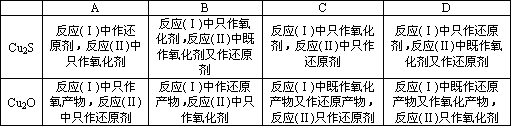
题目内容
根据下列反应判断相关物质还原性由强到弱的顺序是( )H2SO3+I2+H2O══H2SO4+2HI 2FeCl3+2HI══2FeCl2+2HCl+I2
3FeCl2+4HNO3══2FeCl3+NO↑+2H2O+Fe(NO3)3
A.H2SO3>I->Fe2+>NO B.I->Fe2+>H2SO3>NO
C.Fe2+>I->H2SO3>NO D.NO>Fe2+>H2SO3>I-
答案:B
解析:
解析:
| 氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物,即左>右,可由方程式作出判断,如由第一个方程式知:还原性:H2SO3>HI。
|

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)请完成该反应的化学方程式:(系数按顺序填在答题卷上)
C+ KMnO4+ H2SO4→ CO2↑+ MnSO4+ K2SO4+ H2O
(2)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式:
(3)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,E和F均为空气的组成成分.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①写出NO与活性炭反应的化学方程式 .
②根据上述信息判断,温度T1和T2的关系是(填序号) .
a.T1>T2 b.T1<T2 c.无法比较
(4)CO2经常用氢氧化钠溶液来吸收,现有0.4molCO2,若用200mL 3mol/L NaOH溶液将其完全吸.回答下列问题:
①所得溶液的溶质是 (填化学式).
②溶液中下列关系正确的是 (填字母序号).
a.c(Na+)>c(CO
)>c(OH-)>c(HCO
)
b.c(Na+)>c(HCO
)>c(CO
)>c(OH-)
c.c(Na+)=2c(CO
)+c(HCO
)+c(H2CO3)
d.c(H+)+c(Na+)=c(OH-)+2c(CO
)+c(HCO
)
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=3.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的一定浓度的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为1.9×10-4mol/L,则混合后若生成沉淀所需原CaCl2溶液的最小浓度为 .
(1)请完成该反应的化学方程式:(系数按顺序填在答题卷上)
(2)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式:
(3)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,E和F均为空气的组成成分.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
| 物质 温度 |
活性炭(mol) | NO(mol) | E(mol) | F(mol) |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②根据上述信息判断,温度T1和T2的关系是(填序号)
a.T1>T2 b.T1<T2 c.无法比较
(4)CO2经常用氢氧化钠溶液来吸收,现有0.4molCO2,若用200mL 3mol/L NaOH溶液将其完全吸.回答下列问题:
①所得溶液的溶质是
②溶液中下列关系正确的是
a.c(Na+)>c(CO
2- 3 |
- 3 |
b.c(Na+)>c(HCO
- 3 |
2- 3 |
c.c(Na+)=2c(CO
2- 3 |
- 3 |
d.c(H+)+c(Na+)=c(OH-)+2c(CO
2- 3 |
- 3 |
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=3.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的一定浓度的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为1.9×10-4mol/L,则混合后若生成沉淀所需原CaCl2溶液的最小浓度为
化学平衡状态I、II、Ⅲ的相关数据如下表:
根据以上信息判断,下列结论错误的是( )
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| Ⅰ | Fe(s)+CO2?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| Ⅱ | CO(g)+H2O(g)?CO2(g)+H2(g) | K2 | 1.62 | b |
| Ⅲ | Fe(s)+H2O(g)? FeO(s)+H2(g) |
K3 | a | 1.68 |
| A、a>b |
| B、增大压强;平衡状态II不移动 |
| C、升高温度平衡状态Ⅲ向正反应方向移动 |
| D、反应Ⅱ,Ⅲ均为放热反应 |
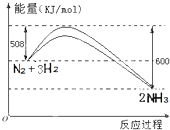 根据要求回答下列叙述相关问题
根据要求回答下列叙述相关问题