题目内容
氢化钠(NaH)是一种还原性极强的物质,广泛应用于工业生产。
(1)氢化钠(NaH)中氢元素的化合价为 。
(2)NaH能与水剧烈反应:NaH+H2O= NaOH+H2↑,该反应中的氧化剂是 。如果有12gNaH与水反应,则转移电子的个数为 。
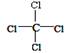
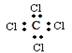
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为 。
(1)氢化钠(NaH)中氢元素的化合价为 。
(2)NaH能与水剧烈反应:NaH+H2O= NaOH+H2↑,该反应中的氧化剂是 。如果有12gNaH与水反应,则转移电子的个数为 。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为 。
(1)—1(共1分)
(2)H2O 3.01×1023或0.5NA(共3分;第一空1分,第二空2分)
(3)2NaH+TiCl4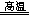 Ti+2NaCl+2HCl↑或4NaH+TiCl4
Ti+2NaCl+2HCl↑或4NaH+TiCl4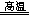 Ti+4NaCl+2H2↑(共2分)
Ti+4NaCl+2H2↑(共2分)
(2)H2O 3.01×1023或0.5NA(共3分;第一空1分,第二空2分)
(3)2NaH+TiCl4
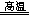 Ti+2NaCl+2HCl↑或4NaH+TiCl4
Ti+2NaCl+2HCl↑或4NaH+TiCl4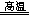 Ti+4NaCl+2H2↑(共2分)
Ti+4NaCl+2H2↑(共2分)试题分析:(1)化合物中钠元素为+1价,由化合价代数和为0可知,氢元素为—1价;(2)氢元素既由—1价升为0价,又由+1价降为0价,既被氧化又被还原,则 NaH是还原剂,H2O是氧化剂;由m/M可知,n(NaH)=0.5mol;由化合价升降总数为1可知,NaH~e—,则该反应转移0.5mol电子,由n?NA可知,N(e—)=3.01×1023或0.5NA;(3)钛元素由+4价降低到0价,由此推测氢元素由—1价升高为0价或+1价,由化合价升价总数相等、原子守恒可知,2NaH+TiCl4
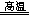 Ti+2NaCl+2HCl↑或4NaH+TiCl4
Ti+2NaCl+2HCl↑或4NaH+TiCl4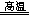 Ti+4NaCl+2H2↑。
Ti+4NaCl+2H2↑。
练习册系列答案
相关题目


 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑ 4NO+6H2O
4NO+6H2O