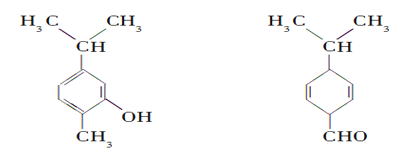题目内容
【题目】指甲花中存在的β-紫罗蓝酮属于一种萜类化合物,可作为合成维生素A的原料。下列有关β-紫罗蓝酮的说法正确的是
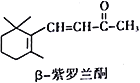
A. β-紫罗蓝酮的分子式为C10H14O
B. 分子中所有碳原子可能处于同一平面
C. 与足量的H2反应后,分子中官能团的种类减少一种
D. 和酸性KMnO4溶液、溴的四氯化碳溶液发生的反应类型相同
【答案】C
【解析】A. 由β-紫罗蓝酮的结构简式可知,该物质的分子式为C13H20O,故A错误;B. 由β-紫罗蓝酮的结构简式可知,β-紫罗蓝酮分子中含有多个饱和碳原子,分子中所有碳原子不可能处于同一平面,故B错误;C. 与足量的H2反应后,分子中碳碳双键发生加成反应而消失,羰基发生加成反应变成羟基,官能团种类由两种变为一种,故C正确;D.β-紫罗蓝酮和酸性KMnO4溶液发生氧化反应,和溴的四氯化碳溶液发生加成反应,反应类型不同,故D错误;答案选C。

练习册系列答案
相关题目