��Ŀ����
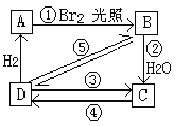
����Ŀ��������ȩ����PTT���������ͻ�����M ��ij�ֺϳ�·�����£�

�ش��������⣺
��1��A�й���������Ϊ______.
��2��B����C�ķ�Ӧ����Ϊ_______��
��3��C�Ľṹ��ʽΪ_______��D��ѧ������_______��
��4����D����PTT�Ļ�ѧ����ʽΪ____________________��
��5�����㻯����W��M��ͬ���칹�壬������Һ����FeCl3��Һ����ɫ��W����______������������ṹ�������к˴Ź�������Ϊ�����Ľṹ��ʽΪ_________��
��6�����������ϳ�·�ߣ����Ҵ���1��3-����ϩΪԭ���������Լ���ѡ��������Ʊ��ϳ� ·��___________________��
·��___________________��
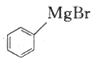
���𰸡� ȩ�� �ӳɷ�Ӧ 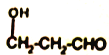 1,3-������
1,3-������ 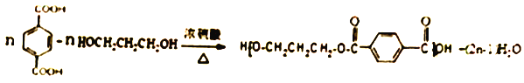 9
9 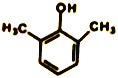
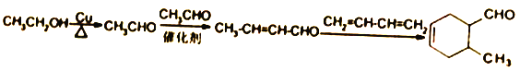
�����������⿼���л�����ƶϺͺϳɣ���1��AΪ��ȩ�����й�������ȩ������2���Ա�B��C�ķ���ʽ��C��B����һ��H2O��˵��B����C�����ӳɷ�Ӧ������D�Ľṹ��ʽ���Ƴ�H2O���ǻ��ӳɵ���ԭ�ӽ϶�IJ�����̼ԭ���ϣ���C�Ľṹ��ʽΪCH2OHCH2CHO����3�����ݣ�2���ķ�����C�Ľṹ��ʽΪCH2OHCH2CHO�����ݺϳ�·�ߣ�C�����������ӳɷ�Ӧ����D����D�Ļ�ѧ����Ϊ1��3������������4��PTT�Ǿ�����Ӧ��D�������۷�Ӧ���ɣ���ѧ��Ӧ����ʽΪ��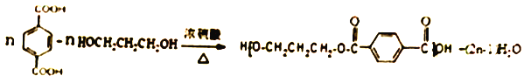 ����5��M�ķ���ʽΪC8H10O����Һ�е���FeCl3��Һ����ɫ��˵�����з��ǻ�������Ҫ���ͬ���칹����
����5��M�ķ���ʽΪC8H10O����Һ�е���FeCl3��Һ����ɫ��˵�����з��ǻ�������Ҫ���ͬ���칹����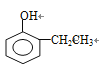 ���ڼ�����֣���
���ڼ�����֣���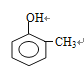 ����һ������4��λ��ȡ������
����һ������4��λ��ȡ������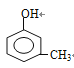 ����һ������2��λ��ȡ����������9�֣��˴Ź���������4��壬˵����4�ֲ�ͬ��ԭ�ӣ�����������Ľṹ��ʽΪ
����һ������2��λ��ȡ����������9�֣��˴Ź���������4��壬˵����4�ֲ�ͬ��ԭ�ӣ�����������Ľṹ��ʽΪ ����6������Ŀ�����Ƴ�����Ŀ�����ķ�Ӧ����CH3CH=CHCHO��CH2=CH��CH=CH2������A����B��ԭ����������ȩ��������CH3CH=CHCHO���Ҵ���������CH3CHO����˺ϳ�·����
����6������Ŀ�����Ƴ�����Ŀ�����ķ�Ӧ����CH3CH=CHCHO��CH2=CH��CH=CH2������A����B��ԭ����������ȩ��������CH3CH=CHCHO���Ҵ���������CH3CHO����˺ϳ�·���� ��
��

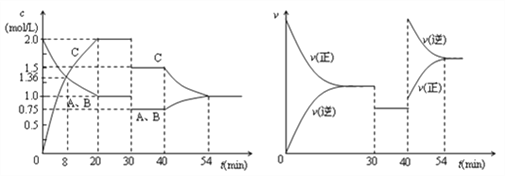
����Ŀ����2 L�ܱ������ڣ�800 ��ʱ��Ӧ2NO(g)��O2(g) 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����ʾ��
ʱ��/(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)�ڵ�5 sʱ��NO��ת����Ϊ_________________________________��
(2)��ͼ�б�ʾNO2�仯���ߵ���______________________��
��O2��ʾ0��2 s�ڸ÷�Ӧ��ƽ������v��______________________��

(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
����Ŀ����ʽ������(NiOOH)�����������ص��������ϣ����÷�����������Ҫ��Ni��Al������Cr��FeS ��)���Ʊ����乤���������£�

�ش��������⣺
(1)�����ݳ�����ʱ��������Ӧ�����ӷ�Ӧ����ʽΪ_________________________;
(2)���ܽ⡱ʱ�ų�������Ϊ_______________ (�ѧʽ);
(3)��֪�������½������ӿ�ʼ��������ȫ������pH���±���
��ʼ������pH | ��ȫ������pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
����pH 1��ʱ����ҺpH��ΧΪ______________________��
(4)�ڿ����м���Ni(OH)2�ɵ�NiOOH,��д���˷�Ӧ�Ļ�ѧ����ʽ_____________;

(5)����������Һ���ж��ִ�����ʽ, CrO42����Cr2O72������Һ�п��ת���������£���ʼŨ��Ϊ1.0mol/L��Na2CrO4��Һ��c(Cr2O72��)��c(H+)�ı仯��ͼ��ʾ�������ӷ���ʽ��ʾNa2CrO4��Һ�е�ת����Ӧ________________������A�����ݼ������ת����Ӧ��ƽ�ⳣ��Ϊ______________,�¶����ߣ���Һ��CrO42����ƽ��ת���ʼ�С����÷�Ӧ�ġ�H____0���>������<����=������