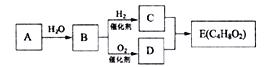
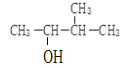
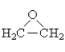
题目内容
【题目】将4molA气体和2molB气体充入到1L的密闭容器中,在一定条件下发生如下反应:2A(g)+ B(g)2C(g)。经2s后达到平衡时,测得C的物质的量为1.2 mol。下列说法中正确的是
A.平衡时,A物质的浓度为2.8 mol·L-1
B.平衡时,B的转化率为70%
C.反应后混合气体的总物质的量为5.2mol
D.用C表示平均反应速率为1.2mol·L-1·s-1
【答案】A
【解析】
根据题干信息,将4molA气体和2molB气体充入到IL的密闭容器中,在一定条件下发生如下反应:2A(g)+ B(g)2C(g)。经2s后达到平衡时,测得C的物质的量为1.2 mol,则C转化的物质的量为1.2mol,列三段式有:

据此分析结合选项解答。
A.根据上述分析可知,平衡时A的物质的量为2.8mol,则A的浓度为![]() ,A选项正确;
,A选项正确;
B.平衡时B转化的物质的量为0.6mol,则B的转化率为![]() ,B选项错误;
,B选项错误;
C.反应后混合气体的总物质的量为2.8+1.4+1.2=5.4mol,C选项错误;
D.2s达到平衡时,C消耗的物质的量为1.2mol,则用C表示平均反应速率为 ,D选项错误;
,D选项错误;
答案选A。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。实验方案如下:

(1)写出滤液A中加入足量硫酸后所发生反应的离子方程式:__________________。
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全。下列物质中可用作调整溶液C的pH的试剂是________(填序号)。
A.铜粉 | B.氨水 | C.氢氧化铜 | D.碳酸铜 |
(3)常温,若溶液C中金属离子均为1 mol·L-1,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20。控制pH=4,溶液中c(Fe3+)=____________,此时________Cu(OH)2沉淀生成(填“有”或“无”)。
(4)将20 mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液80 mL混合,反应的离子方程式为_______________。