题目内容
7.农药在农业生产中起到了重要的作用,有机物D是生产农药的中间体,如下是由A合成有机物D的生产流程.
已知:

(1)A为苯的同系物,其含氢的质量分数与甘油的相等,则A的结构简式是
 .
.(2)有机物C通过连续氧化可以得到一种羧酸E,C与E发生化学反应的方程式是
 ;有机物C还具有的性质有bd
;有机物C还具有的性质有bda、能与氢氧化钠反应 b、能与浓氢溴酸反应c、能发生消去反应d、能发生加成反应
(3)请写出符合下列要求E的同分异构体的结构简式:
①苯环上只有一个取代基的结构简式为
 ;
;②苯环上有两个取代基,且该分子核磁共振氢谱图上有四个吸收峰的结构简式为
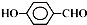 .
.
分析 A为苯的同系物,其含氢的质量分数与甘油的相等,甘油中H元素质量分数=$\frac{8}{36+8+48}$=$\frac{2}{23}$,设A的分子式为CnH2n-6,A中H元素质量分数=$\frac{2n-6}{12n+2n-6}$=$\frac{2}{23}$,n=7,则A为 ;
;
A反应生成B,B发生水解反应生成C,C能连续被氧化生成羧酸E,则C是苯甲醇,结构简式为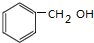 ,B为卤代烃,E为
,B为卤代烃,E为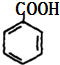 ,C和ClCOCl发生取代反应生成D,D为
,C和ClCOCl发生取代反应生成D,D为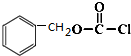 ,据此分析解答.
,据此分析解答.
解答 解:A为苯的同系物,其含氢的质量分数与甘油的相等,甘油中H元素质量分数=$\frac{8}{36+8+48}$=$\frac{2}{23}$,设A的分子式为CnH2n-6,A中H元素质量分数=$\frac{2n-6}{12n+2n-6}$=$\frac{2}{23}$,n=7,则A为 ;
;
A反应生成B,B发生水解反应生成C,C能连续被氧化生成羧酸E,则C是苯甲醇,结构简式为 ,B为卤代烃,E为
,B为卤代烃,E为 ,C和ClCOCl发生取代反应生成D,D为
,C和ClCOCl发生取代反应生成D,D为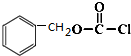 ,
,
(1)通过以上分析知,A为 ,故答案为:
,故答案为: ;
;
(2)在浓硫酸作催化剂、加热条件下,苯甲醇和苯甲酸发生酯化反应生成苯甲酸苯甲酯和水,反应方程式为 ,C为苯甲醇,
,C为苯甲醇,
a、苯甲醇没有所需,所以不能与氢氧化钠反应,故错误;
b、苯甲醇含有醇羟基,能与浓氢溴酸发生取代反应生成卤代烃,故正确;
c、连接醇羟基碳原子相邻碳原子上不含氢离子,所以不能发生消去反应,故错误;
d、含有苯环,一定条件下能发生加成反应,故正确;
故选bd;
故答案为: ;b、d;
;b、d;
(3)E为 ,
,
①E的同分异构体苯环上只有一个取代基的结构简式为 ,故答案为:
,故答案为: ;
;
②E的同分异构体中苯环上有两个取代基,且该分子核磁共振氢谱图上有四个吸收峰的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,正确判断A结构简式是解本题关键,再结合反应条件、题给信息进行推断,难点是同分异构体结构简式确定,题目难度中等.

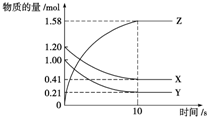 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应在0~10 s内,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应在0~10 s内,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应进行到10 s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为X(g)+Y(g)═Z(g) |
| A. | 常温下,1 L 0.1 mol•L-1 NH4NO3溶液中的氮原子数为0.2NA | |
| B. | 含有58.5 g氯化钠的溶液中含有NA个氯化钠分子 | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA | |
| D. | 常温常压下,22.4 L乙烯中C-H的个数为4NA |
| A. | 0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中c(OH-)=0.1 mol/L,则BA(盐)溶液pH<7 | |
| B. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 | |
| C. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c (Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 4种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小顺序是②>①>③ |
| A. | 加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、SiO32- | |
| B. | 在0.1mol/L氢氧化钠的溶液中:Na+、K+、Cr2O72-、S2- | |
| C. | 在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+ | |
| D. | 在0.1mol/L的硝酸溶液中:NH4+、Ca2+、Cl-、K+ |
| A. | 混合气体的颜色不再变化 | |
| B. | 温度和体积一定时,容器内压强不再变化 | |
| C. | 1molH-H键生成的同时有2molH-I键断裂 | |
| D. | 各物质的物质的量浓度之比为2:1:1 |
| 实验步骤 | 实验现象 |
| ①取少量甲溶液,滴加几滴甲基橙 | 溶液变红色 |
| ②取少量甲溶液,滴加Ba(NO3)2溶液 | 溶液无明显变化 |
| ③取②中实验后的溶液,滴加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ④取少量甲溶液,滴加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(2)实验步骤③的实验结果说明溶液中不存在I-离子
(3)欲确定的离子中肯定存在的是Mg2+、Al3+、Cl-.
(4)为进一步确定其他离子,应该补充的实验是C
A.蒸发 B.过滤C.焰色反应 D.渗析.
| A. | HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(s);△H=-26.5kJ/mol,由此可知I2(s)+H2(g)?2 HI(g);△H=+26.5kJ/mol | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 | |
| D. | 放热反应在常温下一定很容易发生 |