题目内容
某温度下,可逆反应2NO2
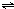
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
(1)此混合气体中NO2与N2O4的物质的量之比.
(2)若反应温度与容器容积不变,开始输进的是N2O4气,从逆向反应达平衡时,求N2O4的转化率.
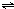
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
(1)此混合气体中NO2与N2O4的物质的量之比.
(2)若反应温度与容器容积不变,开始输进的是N2O4气,从逆向反应达平衡时,求N2O4的转化率.
(1)混合气体的密度是相同条件下氢气的36倍,所以混合气体的平均相对分子质量为36×2=72,
利用十字交叉法计算NO2与N2O4的物质的量之比:
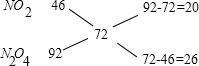
所以n(NO2):n(N2O4)=20:26=10:13,
答:混合气体中NO2与N2O4的物质的量之比为10:13;
(2)与原平衡完全等效,平衡时各组分的物质的量与原平衡相同.
平衡时混合气体中NO2与N2O4的物质的量之比为10:13,令NO2与N2O4的物质的量分别为10mol、13mol.
N2O4
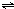
2NO2
开始(mol):13+5=18 0
变化(mol):5 10-0=10
平衡(mol):13 10
所以N2O4的转化率为
×100%=27.8%,
答:N2O4的转化率为27.8%.
利用十字交叉法计算NO2与N2O4的物质的量之比:

所以n(NO2):n(N2O4)=20:26=10:13,
答:混合气体中NO2与N2O4的物质的量之比为10:13;
(2)与原平衡完全等效,平衡时各组分的物质的量与原平衡相同.
平衡时混合气体中NO2与N2O4的物质的量之比为10:13,令NO2与N2O4的物质的量分别为10mol、13mol.
N2O4
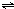
2NO2
开始(mol):13+5=18 0
变化(mol):5 10-0=10
平衡(mol):13 10
所以N2O4的转化率为
| 5mol |
| 18mol |
答:N2O4的转化率为27.8%.

练习册系列答案
相关题目
 N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求: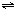 N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求: