题目内容
某温度下,可逆反应2NO2![]() N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍.求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍.求:
(1)此混合气体中NO2和N2O4的物质的量之比.
(2)混合气体中NO2的体积百分含量.
(3)混合气体中NO2和N2O4的质量之比.
(4)若反应的温度与体积不变,开始时输入的气体是N2O4,则平衡时的压强是起始时压强的多少倍?
答案:
解析:
解析:
|
解:(1)M=36×2=72 (2) (3)m(NO2)∶m(N2O4)=46×10∶92×13=5∶13; (4)设开始输进a mol N2O4,转化了x mol 2NO2 起始 0 a 变化 2x x 平衡 2x a-x ∵ |

练习册系列答案
相关题目
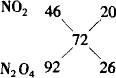 n(NO2)∶n(N2O4)=10∶13;
n(NO2)∶n(N2O4)=10∶13;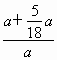 =
= N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
 N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求: