题目内容
【题目】氨基甲酸铵(H2NCOONH4)是一种易水解、受热易分解的白色固体,某研究小组用下图所示的实验装置制备氨基甲酸铵,反应原理为:2NH3(g)+CO2(g)=H2NCOONH4(s) △H<0。
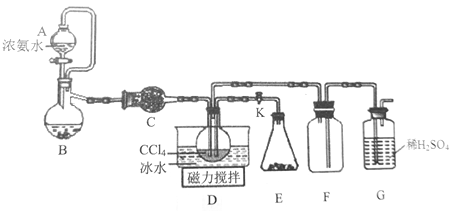
(1)仪器B的名称是________________。
(2)打开阀门K,装置E中由固体药品所产生的气体就立即进入装置D,则该固体药品的名称为________________。
(3)装置D为制备氨基甲酸铵的反应器(CCl4充当惰性介质),在合适催化剂下搅拌一段时间。
①反应在冰水浴中进行的原因为_______________________________________。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,__________(填操作名称)分离得到粗产品。
(4)仪器G的作用有:_______________________________________。
(5)该实验装置中有一处不足,改进方法是______________________________________。
(6)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式_________________。
(7)为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验,已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液):用天平称取一定质量的样品,加水溶解,____________________,测量的数据取平均值进行计算。
【答案】蒸馏烧瓶或具支烧瓶 干冰 防止产品受热分解 过滤 除去过量的氨气,防止污染环境 在D和F之间增加一个装有碱石灰的干燥装置 NH2COONH4+2H2O=NH4HCO3+NH3·H2O或NH2COONH4+2H2O=NH4HCO3+NH3↑ 加入足量Ba(OH)2溶液,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量,重复2~3次
【解析】
在装置B中制取氨气,通过C装置的干燥作用氨气进入到D装置,与由E装置产生的CO2气体发生反应得到产品氨基甲酸铵,氨气是大气污染物,在排放前要进行尾气处理,用G中稀硫酸作吸收试剂,为防止倒吸现象,装置F起安全瓶的作用,以防止倒吸。据此分析解答。
(1)根据图示可知仪器B的名称是蒸馏烧瓶;
(2)装置E的作用是产生CO2气体,若打开阀门K,装置E中由固体药品直接产生CO2,则该固体药品的名称为干冰(即固体CO2),
(3)①在装置D中氨气与CO2气体发生反应:2NH3(g)+CO2(g)=H2NCOONH4(s) △H<0。由于该反应的正反应为气体体积减小的放热反应,反应在冰水浴中就可防止产品受热分解,可以得到更多的固体产物;
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,在装置D中既有反应产生的固体氨基甲酸铵,也有液氨,所以可通过过滤的方法分离得到粗产品;
(4)氨气是大气污染物,在排放前要进行尾气处理,由于氨气的水溶液显碱性,所以仪器G中盛有硫酸,就可以吸收过量的氨气,防止污染环境;
(5)根据图示可知在制取氨基甲酸铵的D装置与尾气吸收的G装置中没有吸收水分的装置,这样稀硫酸中带来的水蒸气就会进入到D中,氨基甲酸铵是弱酸弱碱盐,水和氨基甲酸铵发生水解反应,导致物质变质,所以该实验装置中这一处不足,改进方法是在D和F之间增加一个装有碱石灰的干燥装置;
(6)由于氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式NH2COONH4+2H2O=NH4HCO3+NH3·H2O或写为:NH2COONH4+2H2O=NH4HCO3+NH3↑;
(7)若样品变质,会反应产生NH4HCO3,用天平称取一定质量的样品,加水溶解,配制成溶液,向该溶液中加入足量的Ba(OH)2溶液,发生反应:NH4HCO3+Ba(OH)2=BaCO3↓+NH3↑+2H2O,然后过滤、用蒸馏水洗涤所得沉淀、再干燥后称量沉淀的质量,重复2~3次,即可得到BaCO3的质量,利用反应中的C元素守恒可得NH4HCO3的质量,则NH2COONH4的质量就是样品质量与NH4HCO3的质量差,NH2COONH4的质量除以样品质量,就得到样品中氨基甲酸铵的质量分数。