题目内容
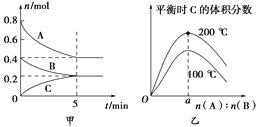
【题目】在容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B.200℃时,该反应的平衡常数为25
C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
【答案】B
【解析】
试题分析:由图甲可知,反应中A、B、C的物质的量的变化量为0.4:0.2:0.2=2:1:1,根据反应中计量数之比等于物质的物质的量的变化量之比可知,该反应方程式为:2A(g)+B(g)![]() C(g),A、根据v=△c/t可知v(B)=
C(g),A、根据v=△c/t可知v(B)=![]() =0.02molL-1min-1,A错误;B、由图可知平衡时A、B、C的物质的量分别为0.4mol、0.2mol、0.2mol,所以它们的浓度分别为:0.2mol/L、0.1mol/L、0.1mol/L,结合化学方程式2A(g)+B(g)
=0.02molL-1min-1,A错误;B、由图可知平衡时A、B、C的物质的量分别为0.4mol、0.2mol、0.2mol,所以它们的浓度分别为:0.2mol/L、0.1mol/L、0.1mol/L,结合化学方程式2A(g)+B(g)![]() C(g),可知该反应的平衡常数为
C(g),可知该反应的平衡常数为![]() =25 L2/mol2,B正确;C、根据图乙可知,升高温度,C的体积分数增大,平衡正向移动,所以正反应为吸热反应,所以升高温度平衡正向移动,同时反应速率增大,C错误;D、根据图乙可知,升高温度,C的体积分数增大,平衡正向移动,所以正反应为吸热反应,△H>0;当投入的反应物的物质的量之比等于化学反应中计量数之比时,平衡时C的体积分数达最大值,根据化学方程式2A(g)+B(g)
=25 L2/mol2,B正确;C、根据图乙可知,升高温度,C的体积分数增大,平衡正向移动,所以正反应为吸热反应,所以升高温度平衡正向移动,同时反应速率增大,C错误;D、根据图乙可知,升高温度,C的体积分数增大,平衡正向移动,所以正反应为吸热反应,△H>0;当投入的反应物的物质的量之比等于化学反应中计量数之比时,平衡时C的体积分数达最大值,根据化学方程式2A(g)+B(g)![]() C(g),可知a=2,D错误;答案选D。
C(g),可知a=2,D错误;答案选D。
【名师点晴】该题解题的关键是先要根据图像写出化学方程式,注意化学平衡图像题的解题技巧:(1)紧扣特征,弄清可逆反应的正反应是吸热还是放热,体积增大、减小还是不变,有无固体、纯液体物质参与反应等。(2)先拐先平,在含量(转化率)—时间曲线中,先出现拐点的则先达到平衡,说明该曲线反应速率快,表示温度较高、有催化剂、压强较大等。(3)定一议二,当图像中有三个量时,先确定一个量不变,再讨论另外两个量的关系,有时还需要作辅助线。