题目内容
某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。实验②的反应物应为
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | | 无 |
| ③ | 10 mL 5% H2O2溶液 | MnO2固体 |
A.5 mL 2% H2O2溶液 B.10 mL 5% H2O2溶液
C.10 mL 2% H2O2溶液 D.5 mL 10% H2O2溶液
B
解析试题分析:根据定一议二的原则可知,在实验①②中均没有使用催化剂,因此改变的条件应该是双氧水的浓度。由于所以③中使用了催化剂,所以实验②③中改变的条件是催化剂,这说明实验②中反应物与实验③中反应物完全相同,所以实验②的反应物应该是10 mL 5% H2O2溶液,答案选B。
考点:考查外界条件对反应速率影响的实验探究

练习册系列答案
相关题目
在四个不同的容器中,分别进行不同条件下的合成氨反应N2(g)+3H2(g) 2NH3(g)。在相同时间内表示该反应速率最快的是
2NH3(g)。在相同时间内表示该反应速率最快的是
| A.v(H2)=0.1 mol/(L·s) | B.v(N2)=0.1 mol/(L·s) |
| C.v(N2)=0.2 mol/(L·s) | D.v(NH3)=0.3 mol/(L·s) |
500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平衡2NO2(g) N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
| A.平衡向正反应方向移动 |
| B.平衡常数K增大 |
| C.NO2的转化率变小 |
| D.容器内气体颜色先变深后变浅,最后比原来还要浅 |
在1L密闭容器中,把l mol A和1 mol B混合发生如下反应:
3A(g) + B(g)  XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是
XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是
| A.x的值为2 | B.A的转化率为40% |
| C.B的平衡浓度为0.8 mol/L | D.达到平衡时D的体积分数为20% |
下列关于化学平衡常数(K),电离平衡常数(Ka或Kb),水解平衡常数(Kh),沉淀溶解平衡常数(Ksp),水的离子积常数(Kw)的叙述中错误的是
| A.K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完全了 |
| B.比较Ksp与离子积Qc的相对大小,可判断难溶电解质在给定条件下沉淀能否生成或溶解 |
| C.K、Ka或Kb、Kh、Ksp、Kw都与温度有关,温度越高,常数值越大 |
| D.弱酸HA的Ka与NaA的Kh、水的离子积常数Kw三者间的关系可表示为:Kw=Ka ·Kh |
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,不能说明反应
A(s)+2B(g) C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
| A.混合气体的压强 | B.混合气体的密度 |
| C.B的物质的量浓度 | D.气体的平均相对分子质量 |
相同温度下,容积相同的甲、乙两个恒容密闭容器中均发生如下反应:2SO2(g) + O2(g)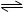 2SO3(g) + 197 kJ实验测得有关数据如下:
2SO3(g) + 197 kJ实验测得有关数据如下:
| 容器编号 | 起始时各物质的物质的量 / mol | 达到平衡时体系能量的变化/KJ | ||
| SO2 | O2 | SO3 | ||
| 甲 | 2 | 1 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 放出热量:Q2 |
下列判断中不正确的是
A.197>Q1>Q2
B.达到平衡时SO2的体积分数:甲>乙
C.两容器中反应的平衡常数相等
D.生成1molSO3(l)时放出的热量大于98.5kJ