题目内容
下列化学用语或模型表示不正确的是
A.中子数为14的硅原子: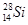 |
B.CH4分子的比例模型: |
C.聚乙烯的结构简式: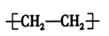 |
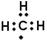
| D.次氯酸分子的结构式:H—O-Cl |
C
试题分析:A、在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数,又因为质子数+中子数=质量数,硅元素的质子数是14,所以中子数为14的硅原子:
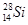 i,A正确;B、甲烷是正四面体型分子,其比例模型是
i,A正确;B、甲烷是正四面体型分子,其比例模型是 ,B正确;C、乙烯加聚得到聚乙烯,结构简式为
,B正确;C、乙烯加聚得到聚乙烯,结构简式为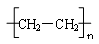 ,C不正确;D、在次氯酸分子中氯原子与氢原子分别与氧原子形成1对共用电子对,D正确,答案选C。
,C不正确;D、在次氯酸分子中氯原子与氢原子分别与氧原子形成1对共用电子对,D正确,答案选C。
练习册系列答案
相关题目
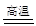 2Fe + Al2O3,下列说法中正确的是( )
2Fe + Al2O3,下列说法中正确的是( )