题目内容
25℃时,用0.1000 mol·L-1 KOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液,滴定中pH变化如图,下列关系错误的是

A.V=0.00mL时,CH3COOH溶液pH=3,其电离平衡常数K≈10-5mol·L-1
B.V=10.00mL时,溶液中c(CH3COO-)>c(K+)>c(H+)>c(OH-)
C.溶液pH=7时,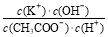 =1
=1
D.V≥20.00mL时,溶液中c(K+)=c(CH3COO—)+c(OH-)+c(CH3COOH)
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
利用下图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是

选项 | a | b | c | c试管中现象 |
A | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液变棕黄色 |
B | 稀硫酸 | Na2S2O3 | 溴水 | 产生浅黄色沉淀 |
C | 硼酸 | Na2CO3 | Na2SiO3溶液 | 析出白色沉淀 |
D | 浓硝酸 | 铁片 | KI-淀粉溶液 | 溶液变蓝色 |


 CO32-+H3O+
CO32-+H3O+
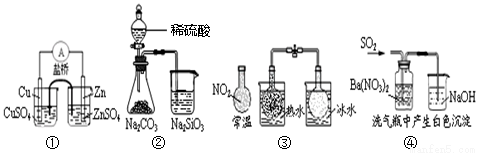
 Zn、Cu原电池 B.② 能证明非金属性:S>C>Si
Zn、Cu原电池 B.② 能证明非金属性:S>C>Si N2O4 △H<0 D.④ 白色沉淀为BaSO3
N2O4 △H<0 D.④ 白色沉淀为BaSO3