题目内容
常温下,下列溶液中各微粒浓度关系不正确的是( )
A、PH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,C(Na+)大小关系:①>③>②
B、向氨水中滴加稀硫酸至溶液呈中性:C(NH4+)>C(SO42-)>C(OH-)=C(H+)
C、向1L 0.1mol/L的NaOH溶液中通入6.6gCO2:2C(Na+)=3[C(CO32-)+C(HCO3-)+C(H2CO3)]
D、 CH3COONa溶液中加入少量KNO3后的碱性溶液一定有:C(Na+)+C(H+)=C(CH3COO-)+C(OH-)
C
【解析】
试题分析: A.阴离子水解程度大小关系是CH3COO-<HCO3-<C6H5O-,等pH的这三种盐溶液,盐浓度大小顺序是:①>③>②,所以C(Na+)大小关系:①>③>②,正确;B.溶液呈中性,则C(OH-)=C(H+),溶液中存在电荷守恒C(NH4+)+C(H+)=2C(SO42-)+C(OH-),所以C(NH4+)=2C(SO42-),正确;C.氢氧化钠的物质的量是0.1mol,n(CO2)=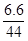 mol=0.15mol,氢氧化钠和二氧化碳的物质的量之比是0.1mol:0.15mol=2:3,所以二氧化碳和氢氧化钠发生的反应为CO2+NaOH=NaHCO3,二氧化碳有剩余,溶液中的溶质是碳酸氢钠,根据物料守恒得C(Na+)=C(CO32-)+C(HCO3-)+C(H2CO3),错误;D.溶液中存在电荷守恒C(Na+)+C(H+)+c(K+)=C(CH3COO-)+C(OH-)+C(NO3-),硝酸钾是强酸强碱盐,则c(K+)=C(NO3-),所以得C(Na+)+C(H+)=C(CH3COO-)+C(OH-),正确.
mol=0.15mol,氢氧化钠和二氧化碳的物质的量之比是0.1mol:0.15mol=2:3,所以二氧化碳和氢氧化钠发生的反应为CO2+NaOH=NaHCO3,二氧化碳有剩余,溶液中的溶质是碳酸氢钠,根据物料守恒得C(Na+)=C(CO32-)+C(HCO3-)+C(H2CO3),错误;D.溶液中存在电荷守恒C(Na+)+C(H+)+c(K+)=C(CH3COO-)+C(OH-)+C(NO3-),硝酸钾是强酸强碱盐,则c(K+)=C(NO3-),所以得C(Na+)+C(H+)=C(CH3COO-)+C(OH-),正确.
考点: 离子浓度大小的比较;盐类水解的应用;酸碱混合时的定性判断及有关PH的计算.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案