题目内容
【题目】下列装置图或曲线图与对应的叙述相符的是
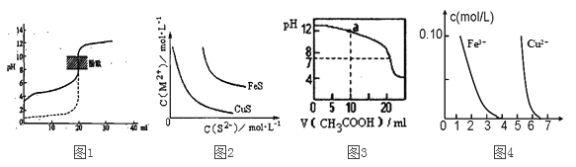
A. 如图1所示,用0.1mol/LNaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线
B. 某温度下FeS、CuS的沉淀溶解平衡曲线如图2所示,纵坐标c(M2+)代表Fe2+或Cu2+的浓度,横坐标c(S2—)代表S2—浓度。在物质的量浓度相等的Fe2+和Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为Fe2+
C. 如图3所示,用0.1mol/LCH3COOH溶液滴定20mL0.1mol/LNaOH溶液的滴定曲线,当pH=7时:c(Na+)=c(CH3COO—)>c(OH—)=c(H+)
D. 据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5.5左右
【答案】C
【解析】A.用0.1mol/LNaOH溶液滴定醋酸时,随着加入氢氧化钠的量的增加,醋酸会电离出一部分氢离子,所以出现的pH值突越要缓慢,故A错误;B.依据图象分析可知,硫化铜溶度积小于硫化亚铁,同浓度Fe2+和Cu2+的溶液中滴加硫化钠溶液,先析出的沉淀是硫化铜,故B错误;C.反应后溶液pH=7,依据溶液中电荷守恒分析,用0.1mol/LCH3COOH溶液滴定20ml0.1mol/LNaOH溶液,反应生成醋酸钠,溶液呈中性,溶液中存在电荷守恒,c(H+)+c(Na+)=c(OH-)+c(CH3COO-),c(H+)=c(OH-),则c(CH3COO-)=c(Na+),得到当pH=7时:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故C正确;D.分析图象可知铁离子完全沉淀的pH为3.7,加入氧化铜会调节溶液pH,到pH=5.5时铜离子会沉淀,应调节溶液pH小于5.5,故D错误;故选C。

【题目】锗![]() 是典型的半导体元素,在电子、材料等领域应用广泛
是典型的半导体元素,在电子、材料等领域应用广泛![]() 回答下列问题:
回答下列问题:
(1)基态Ge原子的核外电子排布式为![]() ______,有______个未成对电子.
______,有______个未成对电子.
(2)![]() 与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键
与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键![]() 从原子结构角度分析,原因是______.
从原子结构角度分析,原因是______.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______.
|
|
| |
熔点 |
| 26 | 146 |
沸点 |
| 186 | 约400 |
(4)光催化还原![]() 制备
制备![]() 反应中,带状纳米
反应中,带状纳米![]() 是该反应的良好催化剂
是该反应的良好催化剂![]() 、Ge、O电负性由大至小的顺序是______
、Ge、O电负性由大至小的顺序是______
![]() 单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
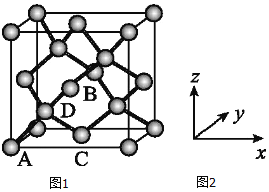
(6)晶胞有两个基本要素: ![]() 原子坐标参数,表示晶胞内部各原子的相对位置,如图
原子坐标参数,表示晶胞内部各原子的相对位置,如图![]() 、
、![]() 为Ge单晶的晶胞,其中原子坐标参数A为
为Ge单晶的晶胞,其中原子坐标参数A为![]() ;B为
;B为![]() ;C为
;C为![]() 则D原子的坐标参数为______.
则D原子的坐标参数为______.
![]() 晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数
晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数![]() ,其密度为______
,其密度为______ ![]() 列出计算式即可
列出计算式即可![]() .
.