题目内容
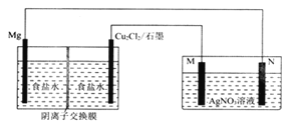
【题目】一种新型镁储备电池的储存寿命长,电压平稳,电池的总反应为Mg+Cu2Cl2=2Cu+MgCl2,以该电池为电源在铜片上镀银的实验装置如图所示。
下列说法正确的是
A. 若反应消耗1mol Mg,则有1mol Cl-通过阴离子交换膜
B. M电极材料为铜片
C. 接通电路后,电池的正极质量减小
D. 接通电路后,AgNO3溶液的浓度减小
【答案】C
【解析】分析:根据电池总反应式可知,Mg为原电池的负极,Cu2Cl2/石墨为原电池的正极,M为电解池的阳极,N为电解池的阴极。
详解:A. 由电荷守恒可知,若反应消耗1mol Mg,则有2mol Cl-通过阴离子交换膜,故A错误;
B. M为电解池的阳极,电极材料应为镀层金属,则M电极材料为Ag,故B错误;
C. 由电池总反应可知,正极反应式为Cu2Cl2+2e-=2Cu+2Cl-,所以接通电路后,电池的正极质量减小,故C正确;
D. 在铜片上镀银时,电解质溶液的组成和浓度均不变,故D错误;答案选C。

练习册系列答案
相关题目