题目内容
【题目】一定温度下,向10 mL H2O2溶液中加入适量FeCl3溶液,反应分两步进行:
①2Fe3++ H2O2=2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+ =2Fe3++2H2O,
反应过程中能量变化如下图所示。下列说法正确的是( )
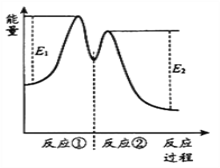
A. 反应②的ΔH=(E2 -E1)kJ·mol-1
B. Fe3+的作用是增大过氧化氢的分解速率
C. 反应2H2O2(aq)=2H2O(l)+O2(g)的△H<0
D. 反应①是放热反应、反应②是吸热反应
【答案】BC
【解析】A.焓变=生成物的总能量-反应物的总能量,整个反应2H2O2(aq) = 2H2O(l)+O2(g)的ΔH=E1-E2,反应②的ΔH=②反应的生成物总能量-②反应的反应物总能量。不等于E1-E2,故A错误;B.根据总反应2H2O2(aq)=2H2O(l)+O2(g),Fe3+是催化剂,其作用是加快过氧化氢的分解速率,故B正确;C.由图知反应物的总能量大于生成物的总能量,所以反应2H2O2(aq)=2H2O(l)+O2(g)为放热反应,故△H<0,故C正确;D.反应①生成物的能量大于反应物的能量是吸热反应,反应②生成物的能量小于反应物的能量是放热反应,故D错误;答案:BC。

 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】能用H++ OH-= H2O来表示的化学反应是( )
A. CuO溶于稀H2SO4 B. 澄清石灰水和HNO3溶液反应
C. KOH溶液和碳酸溶液反应 D. Ba(OH)2溶液和H2SO4溶液反应
【题目】今年6月20日,2016年全球最受关注的十大化学成果发布,其中有两项与空气中的二氧化碳处理利用技术有关。其一为美国伊利诺斯大学芝加哥分校和阿贡国家实验室科学家联合设计的新型太阳能电池,可直接把大气中的二氧化碳转化为合成气(CO和H2)该设计同时具有环保和经济价值,不仅可以减缓二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太阳能电池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
(2)下图装置可实现二氧化碳到一氧化碳的转化

①电源的正极为______(“A”或“B")。
②阴极发生反应的电极方程式为:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285. 8kJ/mol、726.5kJ/mol,写出 由CO和H2制备CH3OH(1)的热化学方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g)=CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
时间(min) | 0 | 1 | 5 | 10 | 30 | 50 |
压强(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
5min内该反应的平均速率用CO可表示为______,该温度下的平衡常数是_____。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,CH3OH的体积分数比原平衡时_____( 填“大”或“小”)。