题目内容
【题目】某科研小组发现有机化合物A的结构如图所示:
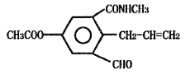
下列有关化合物A说法正确的是
A.化合物A的分子式为C14H13NO4
B.向化合物A中加入少量溴水,观察到溴水褪色,证明化合物A中含碳碳双键
C.1 mol化合物A最多可与3 mol NaOH溶液发生反应
D.化合物A可发生加成、氧化、缩聚、取代等反应
【答案】C
【解析】
A. 通过结构可知,该有机物的不饱和度为8,故分子式为C14H15NO4,A错误;
B. 向化合物A中加入少量溴水,观察到溴水褪色,可能是由于萃取的作用,无法证明其中含碳碳双键,B错误;
C. 该化合物中,![]() 部分在碱性条件下水解,会生成羧酸钠和一分子酚,酚会继续与NaOH发生中和反应,该部分可消耗2molNaOH,化合物中的酰胺键在NaOH条件下也会水解,消耗1molNaOH,则1 mol化合物A最多可与3 mol NaOH溶液发生反应,C正确;
部分在碱性条件下水解,会生成羧酸钠和一分子酚,酚会继续与NaOH发生中和反应,该部分可消耗2molNaOH,化合物中的酰胺键在NaOH条件下也会水解,消耗1molNaOH,则1 mol化合物A最多可与3 mol NaOH溶液发生反应,C正确;
D. 该化合物无法发生缩聚反应,D错误;
故答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是
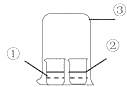
①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D