题目内容
9.常温下,0.1mol•L-1的三种盐溶液NaX、NaY、NaZ的pH分别为 7、8、9,则下列判断中正确的是( )| A. | c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) | B. | 离子浓度:c(Z-)>c(Y-)>c(X-) | ||
| C. | 电离常数:K(HZ)>K(HY) | D. | HX、HY、HZ的酸性依次增强 |
分析 常温下,0.1mol/L的三种盐溶液NaX.NaY.NaZ的PH分别为7、8、9,对于弱酸,其酸性越弱,对应的盐水解程度越大,说明HX为强酸,HY、XZ为弱酸,且酸性HY>XZ,由此分析解答.
解答 解:A、NaX电离后不水解,X-的物质的量浓度c(X-)=0.1mol/L,NaY、NaZ电离后都部分水解,根据物料守恒可知:c(Y-)+c(HY)=0.1mol/L;c(Z-)+c(HZ)=0.1mol/L,所以c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ),故A正确;
B、酸越弱水解的程度越大,离子浓度越小,所以c(X-)>c(Y-)>c(Z-),故B错误;
C、对于弱酸,其酸性越弱,对应的盐水解程度越大,说明HX为强酸,HY、XZ为弱酸,且酸性HX>HY>XZ,电离常数K(HY)>K(HZ),故C错误;
D、对于弱酸,其酸性越弱,对应的盐水解程度越大,说明HX为强酸,HY、XZ为弱酸,且酸性HX>HY>XZ,故D错误;
故选A.
点评 本题考查盐类的水解,题目难度中等,注意酸根离子水解程度越大,对应的酸越弱.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.为了减少大气中二氧化碳的含量,下列措施不可行的是( )
| A. | 改进能源结构 | B. | 提高能源利用率 | ||
| C. | 大量使用化石燃料 | D. | 提倡植树种草 |
20.某实验小组在同样的实验条件下,用同样的实验仪器和方法步骤进行两组综合热测定的实验,实验试剂及其用量如表所示:
(1)实验①中碱液过量的目的是使盐酸充分反应,提高实验的准确度.
(2)甲同学预计△H1≠△H2,其依据是NH3•H2O是弱电解质,存在电离平衡,电离过程是吸热程.
(3)上表中终了温度为反应过程中混合溶液的最高温度(填“最高温度”或“平均温度”).
(4)在中和热测定实验中,若测定硫酸的温度计未用水洗涤就直接测量碱溶液的温度,则测得的中和热△H偏大(填“偏大”“偏小”或“不变”,下同).
(5)若实验①中硫酸用盐酸代替,且中和反应时有少量HCl挥发,则测得中和反应过程中放出的热量Q偏小.
| 反应物 | 起始温度/℃ | 终了温度/℃ | 中和热/kJ•mol-1 | |
| 硫酸 | 碱溶液 | |||
| ①0.5 mol•L-1 H2SO4溶液50 mL、1.0 mol•L-1 NaOH溶液50 mL | 25.1 | 25.1 | △H1 | |
| ②0.5 mol•L-1 H2SO4溶液50 mL、1.1mol•L-1 NH3•H2O溶液50 mL | 25.1 | 25.1 | △H2 | |
(2)甲同学预计△H1≠△H2,其依据是NH3•H2O是弱电解质,存在电离平衡,电离过程是吸热程.
(3)上表中终了温度为反应过程中混合溶液的最高温度(填“最高温度”或“平均温度”).
(4)在中和热测定实验中,若测定硫酸的温度计未用水洗涤就直接测量碱溶液的温度,则测得的中和热△H偏大(填“偏大”“偏小”或“不变”,下同).
(5)若实验①中硫酸用盐酸代替,且中和反应时有少量HCl挥发,则测得中和反应过程中放出的热量Q偏小.
17.用下列物质冶炼相应金属时采用电解法的是( )
| A. | Fe2O3 | B. | Ag2O | C. | Cu2S | D. | Al2O3 |
4.下列说法正确的是( )
| A. | 硅的化学性质不活泼,常温下不与任何物质反应 | |
| B. | 酸性氧化物都只能与碱反应不能与任何酸发生反应 | |
| C. | 工业上用焦炭和石英制取粗硅的反应方程式为SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| D. | 不能用SiO2与水反应的方法来制取硅酸,不能用瓷坩埚来加热烧碱或纯碱使其熔化 |
18.下列关于元素周期律和元素周期表的说法中错误的是( )
| A. | 元素周期律的实质是元素原子的核外电子排布呈周期性变化 | |
| B. | 利用元素周期律可以预测元素及其化合物的性质 | |
| C. | 元素周期表有7个横行,也就是7个周期 | |
| D. | 元素周期表有18个纵列,也就是18个族 |
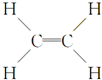 ;
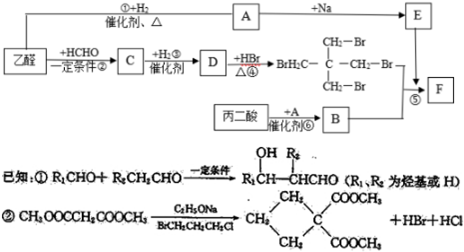
;
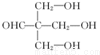 .
. .
. .
. .
.