题目内容
某充电电池的原理如图所示,溶液中c(H+)=2.0mol?L-1,阴离子为SO42-,a、b均为惰性电极,充电时右槽溶液颜色由绿色变为紫色.下列对此电池叙述正确的是( )

| A.放电过程中,左槽溶液颜色由黄色变为蓝色 |
| B.充电时,b极接直流电源正极,a极接直流电源负极 |
| C.充电过程中,a极的反应式为:VO2++2H++e-=VO2++H2O |
| D.放电时,当转移1.0mol电子时共有1.0molH+从左槽迁移进右槽 |

A.放电时,a电极为原电池正极,左槽中得电子发生还原反应,所以溶液颜色由黄色变为蓝色,故A正确;
B.充电时,b电极为阴极,a极为阳极,则b极接直流电源负极,a极接直流电源正极,故B错误;
C.充电过程中,a极是电解池阳极,a极的反应式为VO2+-e-+H2O=VO2++2H+,故C错误;
D.放电时,阳离子向正极移动,所以氢离子向左槽移动,故D错误;
故选A.
B.充电时,b电极为阴极,a极为阳极,则b极接直流电源负极,a极接直流电源正极,故B错误;
C.充电过程中,a极是电解池阳极,a极的反应式为VO2+-e-+H2O=VO2++2H+,故C错误;
D.放电时,阳离子向正极移动,所以氢离子向左槽移动,故D错误;
故选A.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。
2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。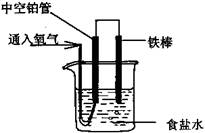


 不能自发进行,则该反应的
不能自发进行,则该反应的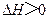
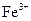 、
、 、
、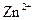 的氧化性依次减弱
的氧化性依次减弱