题目内容
.⑴今有2H2+O2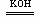 2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。
2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。
⑵如把KOH改为稀H2SO4作电解质,则电极反应式为: 、
。⑴和⑵的电解液不同,反应进行后,其溶液的PH值变化为 、 。
⑶如把H2改为甲烷,KOH作电解质,则负极反应式为: 。
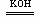 2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。
2H2O反应,设计成燃料电池,则负极通的应是 ,正极通的应是 ,电极反应式为: 、 。⑵如把KOH改为稀H2SO4作电解质,则电极反应式为: 、
。⑴和⑵的电解液不同,反应进行后,其溶液的PH值变化为 、 。
⑶如把H2改为甲烷,KOH作电解质,则负极反应式为: 。
:⑴H2 O2 负极:2H2+4OH-→4H2O+4e-;正极:O2 + 2H2O + 4e-→ 4OH-;⑵负极:2H2→4H++4e-;正极:O2+4H++4e-→2H2O;⑴中变小,⑵中变大;⑶负极:CH4+10OH―=CO32-+7H2O+8e―。
依据原电池的原理应用。首先考虑原电池反应所依据的氧化还原反应,再考虑产物与电解质溶液的反应。⑴⑵两问中原电池反应为2H2+O2=2H2O,最后一问原电池反应为CH4+2O2+2KOH=K2CO3+3H2O。

练习册系列答案
相关题目
 2PbSO4+2H2O 下列叙述正确的是( )
2PbSO4+2H2O 下列叙述正确的是( )