题目内容
【题目】25℃时,向20 mL 0.1 mol/L一元弱酸HA溶液中滴加0.1 mol/L NaOH溶液,溶液中lg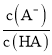 与pH关系如图所示。下列说法正确的是
与pH关系如图所示。下列说法正确的是
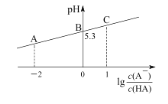
A.A点或B点所示溶液中,离子浓度最大的均是Na+
B.HA滴定NaOH溶液时可用甲基橙作指示剂
C.达到图中B点溶液时,加入NaOH溶液的体积小于10 mL
D.对C点溶液加热(不考虑挥发),则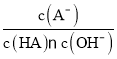 一定增大
一定增大
【答案】C
【解析】
A. 溶液在A、B点时,溶液显酸性,则c(H+)>c(OH-),溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),由于c(H+)>c(OH-),所以c(Na+)<c(A-),故A、B点溶液中离子浓度最大的都不是Na+,A错误;
B. HA为弱酸,NaOH为强碱,HA与NaOH恰好完全反应时生成强碱弱酸盐NaA,由于A-的水解NaA溶液呈碱性,而甲基橙作指示剂时溶液pH变化范围是3.1~4.4,所以HA滴定NaOH溶液时不能选择甲基橙作指示剂,B错误;
C. 溶液在B点时pH=5.3,lg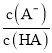 =0,则c(A-)=c(HA),弱酸HA的电离平衡常数Ka=
=0,则c(A-)=c(HA),弱酸HA的电离平衡常数Ka=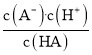 =c(H+)=10-5.3,A-的水解平衡常数Kh=
=c(H+)=10-5.3,A-的水解平衡常数Kh=![]() <10-5.3,若向20 mL0.1mol/L HA溶液中加入10 mL0.1mol/LNaOH溶液,得到的是等浓度的HA、NaA的混合溶液,由于HA的电离程度大于NaA的水解程度,则溶液中c(A-)>c(HA),即lg
<10-5.3,若向20 mL0.1mol/L HA溶液中加入10 mL0.1mol/LNaOH溶液,得到的是等浓度的HA、NaA的混合溶液,由于HA的电离程度大于NaA的水解程度,则溶液中c(A-)>c(HA),即lg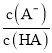 >0,故B点溶液时,加入NaOH溶液的体积小于10 mL,C正确;
>0,故B点溶液时,加入NaOH溶液的体积小于10 mL,C正确;
D. 温度升高,盐水解程度增大,A-的水解平衡常数会增大, 会随温度的升高而减小,D错误;
会随温度的升高而减小,D错误;
故答案选C。

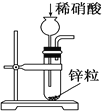
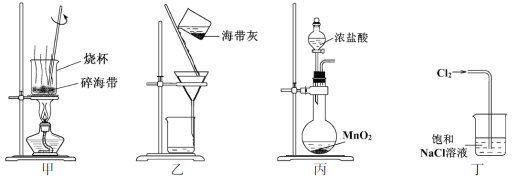
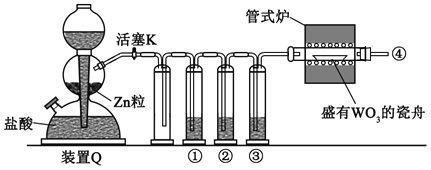
【题目】下列选项中,为完成相应实验,所用仪器或相关操作合理的是( )
A | B | C | D |
配制1mol/L AlCl3溶液 | 实验室制取 氢气 | 比较硫、碳、硅三种 元素的非金属性强弱 | 盛装NaOH 溶液 |
|
|
|
|
A. AB. BC. CD. D