题目内容
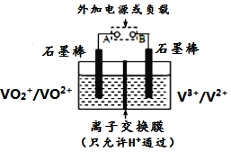
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是 ( )
A. 放电时,右槽电解液pH不变
B. 充电时,阴极电解液pH升高
C. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
D. 充电时,每转移1mol电子,右槽中n(H+)的变化量为1mol
【答案】C
【解析】A.电池放电时,右槽中的电极反应为:V2+-e-=V3+,可知发生氧化反应,选项A错误;B.充电时,阴极发生V3++e-=V2+,H+参加反应,pH不发生变化,选项B错误;C.放电时,左槽发生还原反应,电极方程式应为VO++2H++e-=VO2++H2O,选项C正确;D.充电时,电极反应式为VO2++H2O-e-=VO++2H+,每转移1mol电子,n(H+)的变化量为2mol,选项D错误;答案选C。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
【题目】下列物质的分类组合中正确的是
A | B | C | D | |
强电解质 | Cu(OH)2 | KCl | HCl | CaCO3 |
弱电解质 | NaOH | NH3H2O | BaSO4 | CH3COOH |
非电解质 | SO2 | 金刚石 | NH3 | C2H5OH |
导电物质 | 石墨 | 稀H2SO4 | 熔融KCl | 铜 |
A. A B. B C. C D. D