��Ŀ����
����Ŀ������þ���壨MgSO4��7H2O����һ����Ҫ�Ļ���ԭ�ϡ�����þ����Ҫ�ɷ���MgCO3��������FeCO3�Ͳ��������ʣ�Ϊԭ����ȡ����þ����Ĺ������£�
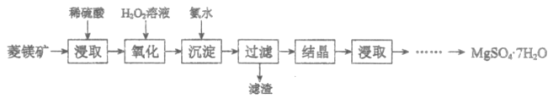
��1��MgCO3����ϡ��������ӷ���ʽ��___________��
��2���������������У�����H2O2��Һ��Ŀ����___________�������ӷ���ʽ��ʾ����
��3���������������У��ð�ˮ������ҺpH�ķ�Χ��___________��
��֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Mg2�� | Fe2�� | Fe3�� |
��ʼ���� | 9.1 | 7.6 | 1.9 |
��ȫ���� | 11.1 | 9.7 | 3.2 |
��4����������������Һ�к��е���������___________��
���𰸡�MgCO3��2H����Mg2����CO2����H2O H2O2��2Fe2����2H����2Fe3����2H2O 3.2~9.1 Mg2����NH4��
��������
�ɻ�ѧ�������̿�֪����þ���ϡ�����ȡ��MgCO3��FeCO3����ϡ��������Mg2+��Fe2+������H2O2��Һ��Fe2+����ΪFe3+��Ȼ��Ӱ�ˮ������ҺpH����Fe3+ת��Ϊ��������������ȥ������Һ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ�MgSO4��7H2O���塣
��1������ǿ��������ԭ����MgCO3����ϡ������������þ��ˮ�Ͷ�����̼�����ӷ���ʽ��MgCO3 + 2H+ = Mg2+ + CO2��+H2O���ʴ�Ϊ��MgCO3 + 2H+ = Mg2+ + CO2��+H2O��
��2������H2O2��Һ��Ŀ���ǽ�Fe2+����ΪFe3+����Ӧ�����ӷ���ʽΪH2O2 + 2Fe2+ + 2H+ = 2Fe3+ + 2H2O���ʴ�Ϊ��H2O2 + 2Fe2+ + 2H+ = 2Fe3+ + 2H2O��
��3���ð�ˮ������ҺpH��ʹFe3+������ȥ������Ӱ��Mg2+����������ݿ�֪��pH=3.2ʱFe3+������ȫ��pH=9.1ʱMg2+��ʼ���������ð�ˮ������ҺpH�ķ�Χ��3.2~9.1���ʴ�Ϊ��3.2~9.1��
��4������������������ʹ�ð�ˮ��ʹFe3+������ȥ����Mg2+û�г����������������Һ�д��ڴ�������������Mg2+��NH4+���ʴ�Ϊ��Mg2+��NH4+��