��Ŀ����
����Ŀ����������к���Cr��OH��3��Al2O3��ZnO��CuO��NiO�����ʣ���ҵ��ͨ���������̻���Na2Cr2O7�����ʣ� 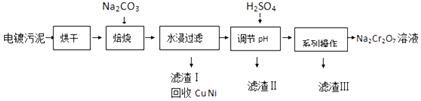
��֪��
��Cr��OH��3��ZnO��Al2O3һ����Ϊ���Ի����
��Na2Cr2O7��Na2SO4�ڲ�ͬ�¶��µ��ܽ�������
20�� | 60�� | 100�� | |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
��1�����չ���������Na2CrO4�Ļ�ѧ����ʽΪ��ˮ������Һ�г�Na2CrO4�����ڵ�����������
��2������H2SO4����pH��Ŀ��Ϊ��
��3���õ�������ġ�ϵ�в������IJ���Ϊ�����ˣ�
��4����1L����H2SO4��������Һ�к���Ԫ������Ϊ23.4g��CrO42����8/9ת��ΪCr2O72�� �� ��ת����������Һ��c��Cr2O72����=molL��1��
��5����Na2Cr2O7��H2SO4���Һ�м���H2O2 �� �ټ������Ѳ�ҡ�������Ѳ�Ϊ��ɫ������������CrO5 �� ������Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1��4Cr��OH��3+4Na2CO3+3O2 ![]() 4Na2CrO4+6H2O+4CO2��NaAlO2��Na2ZnO2
4Na2CrO4+6H2O+4CO2��NaAlO2��Na2ZnO2
��2����ȥ��Һ��NaAlO2��Na2ZnO2���ʣ�����CrO42��ת��ΪCr2O72��
��3������Ũ������ȴ�ᾧ
��4��0.2
��5��Na2Cr2O7+4H2O2+H2SO4�T2CrO5+Na2SO4+5H2O
���������⣺��1����������ķ�����֪������������̼�����������������±������ɸ����ƣ���Ӧ�Ļ�ѧ����ʽΪ4Cr��OH��3+4Na2CO3+3O2 ![]() 4Na2CrO4+6H2O+4CO2 �� ���պ�Ĺ�����Na2CrO4��Na2ZnO2��NaAlO2������ˮ������ˮ������Һ�е����ʳ�Na2CrO4������ NaAlO2��Na2ZnO2 �� ���Դ��ǣ�4Cr��OH��3+4Na2CO3+3O2
4Na2CrO4+6H2O+4CO2 �� ���պ�Ĺ�����Na2CrO4��Na2ZnO2��NaAlO2������ˮ������ˮ������Һ�е����ʳ�Na2CrO4������ NaAlO2��Na2ZnO2 �� ���Դ��ǣ�4Cr��OH��3+4Na2CO3+3O2 ![]() 4Na2CrO4+6H2O+4CO2�� NaAlO2��Na2ZnO2����2��ˮ������Һ�д���Na2CrO4 �� �������ᷢ��CrO42��+2H+Cr2O72��+H2O��NaAlO2��Na2ZnO2���ᷴӦ�����Գ�ȥ��Һ��NaAlO2��Na2ZnO2���ʣ�����CrO42��ת��ΪCr2O72�� ��
4Na2CrO4+6H2O+4CO2�� NaAlO2��Na2ZnO2����2��ˮ������Һ�д���Na2CrO4 �� �������ᷢ��CrO42��+2H+Cr2O72��+H2O��NaAlO2��Na2ZnO2���ᷴӦ�����Գ�ȥ��Һ��NaAlO2��Na2ZnO2���ʣ�����CrO42��ת��ΪCr2O72�� ��
���Դ��ǣ���ȥ��Һ��NaAlO2��Na2ZnO2���ʣ�����CrO42��ת��ΪCr2O72������3���������м������������ظ����ƺ������ƣ����Եõ�������ӦΪ�����ƣ������������ʵ��ܽ�����¶ȵĹ�ϵ��֪�ظ����Ƶ��ܽ�Ƚϴ������Ƶ��ܽ�Ƚ�С�����Եõ������������ƵIJ���Ϊ ����Ũ������ȴ�ᾧ�����ˣ�
���Դ��ǣ�����Ũ������ȴ�ᾧ����4����1L����H2SO4��������Һ�к���Ԫ������Ϊ23.4g���������ʵ���Ϊ ![]() =0.45mol��CrO42����8/9ת��ΪCr2O72�� �� ������Һ��n��Cr2O72����=0.45mol��
=0.45mol��CrO42����8/9ת��ΪCr2O72�� �� ������Һ��n��Cr2O72����=0.45mol�� ![]() =��
=�� ![]() 0.2 mol������Һ��c��Cr2O72����=0.2molL��1 ��
0.2 mol������Һ��c��Cr2O72����=0.2molL��1 ��
���Դ��ǣ�0.2����5��Na2Cr2O7��H2O2 �� �����������·�Ӧ����CrO5 �� ��Ӧ�Ļ�ѧ����ʽΪNa2Cr2O7+4H2O2+H2SO4�T2CrO5+Na2SO4+5H2O��
���Դ��ǣ�Na2Cr2O7+4H2O2+H2SO4�T2CrO5+Na2SO4+5H2O��