题目内容
【题目】下列不能用平衡移动原理解释的是( )
A.新制氯水中加入CaCO3固体可增大HClO分子的浓度
B.钢铁在潮湿的空气中比在干燥空气中更容易生锈
C.通入过量的空气与SO2反应可以提高SO2的利用率
D.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
【答案】B
【解析】
A. 氯水中存在:Cl2+H2O ![]() H++Cl-+HClO,加入CaCO3与H+反应,平衡正向移动,HClO浓度增大,能用平衡移动原理解释,A项错误;
H++Cl-+HClO,加入CaCO3与H+反应,平衡正向移动,HClO浓度增大,能用平衡移动原理解释,A项错误;
B. 钢铁在潮湿空气中发生电化学腐蚀,与平衡移动原理无关,B项正确;
C. 空气过量,促进平衡正向移动,提高SO2的利用率,能用平衡移动原理解释,C项错误;
D. 加压后,二氧化氮浓度增大,气体颜色变深,然后平衡2NO2![]() N2O4向正反应方向移动,所以又变浅,能用平衡移动原理解释,故D错误;
N2O4向正反应方向移动,所以又变浅,能用平衡移动原理解释,故D错误;
题目要求选不能解释的,故选B。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
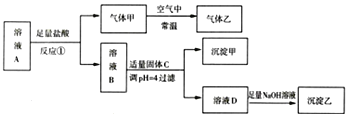
寒假天地重庆出版社系列答案【题目】电石浆是氯碱工业中的一种废弃物,其大致组成如表所示:
成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其它不溶性的物质 |
质量分数/% | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程:
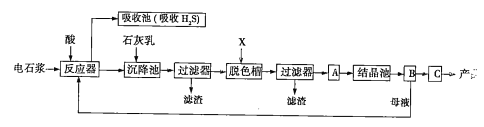
已知氯化钙晶体的化学式是CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中加入的酸应选用______________。
(2)脱色槽中应加入的物质X是__________;设备A的作用是__________;设备B的名称为__________;设备C的作用是_______________。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是_______(填序号)。反应的化学方程式为____________________________。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是______________________。