��Ŀ����
����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷����ɵ�ص�ͭñ(Zn��Cu�ܺ���ԼΪ99%)����ͭ���Ʊ�ZnO�IJ���ʵ��������£�
(1)��ͭñ�ܽ�ʱ����H2O2��Ŀ����___________________(�û�ѧ����ʽ��ʾ)��
��ͭñ�ܽ���轫��Һ�й���H2O2��ȥ����ȥH2O2�ļ�㷽����_________________��
(2)Ϊȷ������п��(��Ҫ�ɷ�ΪZn��ZnO������Ϊ������������)������ʵ������ⶨ��ȥH2O2����Һ��Cu2+�ĺ�����ʵ�����Ϊ��ȷȡһ������ĺ���Cu2+����Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㡣���������е����ӷ���ʽ���£�2Cu2++4I-=2CuI(��ɫ)��+I2 I2+2S2O32-=2I-+S4O62-
�ٵζ�ѡ�õ�ָʾ��Ϊ_____________���ζ��յ�۲쵽������Ϊ_________________��
�����ζ�ǰ��Һ��H2O2û�г��������ⶨ��Cu2+�ĺ�������__________(�ƫ�ߡ��� ƫ�͡��� ���䡱)��
(3)��֪pH>11ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2-���±��г��˼����������������������pH(��ʼ������pH����������Ũ��Ϊ1.0mol��L-1����)
��ʼ������pH | ��ȫ������pH | |
Fe3+ | 1.1 | 3.2 |
Fe 2+ | 5.8 | 8.8 |
Zn2+ | 5.9 | 8.9 |
ʵ���п�ѡ�õ��Լ���30%H2O2��1.0mol��L-1HNO3��1.0mol��L-1NaOH��
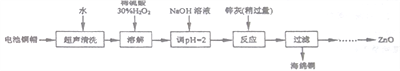
�ɳ�ȥͭ����Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��
������Һ�м���___________ʹ���ַ�Ӧ���ڵμ�1.0mol��L-1���������ƣ�����3.2��pH<5.9��ʹ___________������ȫ���۹��ˣ�������Һ�еμ�1.0 mol��L-1���������ƣ�����pHΪ________��pH��_______��ʹZn2+������ȫ���ݹ��ˡ�ϴ�ӡ������900�����ա�
���𰸡� Cu+H2O2+H2SO4=CuSO4+2H2O ����(����) ������Һ ��ɫ��ȥ��������ڲ��ָ� ƫ�� 30%��H2O2 Fe3+ 8.9 11
�����������÷Ͼɵ�ص�ͭñ(Zn��Cu�ܺ���ԼΪ99%)���� Cu���Ʊ�ZnO,���ͭñ����ˮ���˺��ȥ����ˮ������,�ڹ����м�����������ܽ�,ͭ��������ͭ��Һ,������н���Һ�й�����H2O2��ȥ,��������������Һ������ҺpH=2����������������п��(��Ҫ�ɷ�ΪZn��ZnO,����Ϊ������������),��Ӧ���˵õ�����ͭ,����п���ӵõ�������п,�ּ���ó�������п��(1)������������Cu��������ⷢ��������ԭ��Ӧ��������ͭ��ˮ���ڹ���������ȵ�153������ҵķֽ��� (2)�ٸ��ݵ�����ⵥ�����ñ���������ڸ���H2O2+2I-+2H+=I2+2H2O�����(3)�μ�H2O2��Һ,ʹFe2��ת����ȫΪFe3��,�μ�NaOH��Һ,�γ�������������,���Ӻ��γ�������п����,���ˡ�ϴ�ӡ�����900�������Ƶ�����п��
���: (1)����Ϊ˫��ˮ��������Һ���Ȱ�ͭ����������ͭ,��Ȼ����һ�����ķ�Ӧ,�γ�һ��ƽ��,�����γɵ�����ͭ���Ͼͻᱻϡ�����ܽ�,ƽ�ⱻ����,��Ӧ�����������,�ʶ����ܽ�,��Ӧ�Ļ�ѧ����ʽΪ: Cu+H2O2+H2SO4=CuSO4+2H2O����ˣ�������ȷ����: Cu+H2O2+H2SO4=CuSO4+2H2O��
�ڹ����������ʱȽ��ȶ�,�����ȵ�153������ҵķֽ�Ϊˮ������,����Һ�й�����H2O2��ȥ�ɼ�����������ˣ�������ȷ����:����������
(2)�ٵ�����ҺΪָʾ��,�����һ��Na2S2O3��Һ����ʱ,��Һ��ɫ��ȥ,�������ɫ����,˵���ζ������յ�����ˣ�������ȷ������������Һ����ɫ��ȥ��������ڲ��ָ���
��������H2O2,����KI��,�������·�Ӧ: H2O2+2I-+2H+=I2+2H2O����2Cu2++4I-=2CuI(��ɫ)��+I2�����ɵĵ�,ʹ�ⶨ���ƫ������ˣ�������ȷ����:ƫ��.
��ȥͭ����Һ�к���Fe3����Fe2����Zn2���ȣ����Ʊ�ZnOӦ��ȥFe3����Fe2�����ɱ�����Ϣ��֪��Fe2����Zn2����ʼ�����ͳ�����ȫ��pH������С����Fe3����Zn2����ʼ�����ͳ�����ȫ��pH�����ϴʿɼ���30% H2O2��Fe2��������Fe3�����ٵμ�NaOH��Һ��������Һ��pH(3.2��pH<5.9)��ʹFe3��������ȫ����ʱZn2����������������ַ�Ӧ����ˣ�����Һ�еμ�NaOH��Һ��������Һ��pH(8.9��pH��11)��ʹZn2������Zn(OH)2����������Zn(OH)2��������ϴ�ӡ�������գ����ɵõ�ZnO��

����Ŀ����̽��������ˮ�ɷּ����ʵ�ʵ���У��������з������������ܵó���Ӧ���۵���
���� | ���� | ���� | |
A | �۲���ˮ��ɫ | ��ˮ�ʻ���ɫ | ��ˮ�к�Cl2 |
B | ��NaHCO3��Һ�м���������ˮ | ����ɫ������� | ��ˮ�к�HClO |
C | ���ɫֽ���ϵμ���ˮ | ��ɫֽ����ɫ | ��ˮ����Ư���� |
D | ��FeCl2��Һ�еμ���ˮ | ��Һ����ػ�ɫ | ��ˮ���������� |
A. A B. B C. C D. D