题目内容
【题目】熔化氢氧化钠时,应选用的坩埚是( )
A. 铁坩埚 B. 石英坩埚 C. 刚玉坩埚 D. 陶瓷坩埚
【答案】A
【解析】
A.铁坩埚含有铁,铁与氢氧化钠不反应,可以用铁坩埚熔化氢氧化钠,故A正确;
B.石英中含有二氧化硅,二氧化硅能和氢氧化钠反应生成硅酸钠和水,不能用石英坩埚,故B错误;
C.氧化铝能和氢氧化钠反应生成偏铝酸钠和水,不能用刚玉坩埚,故C错误;
D.陶瓷坩埚含有二氧化硅,二氧化硅能和氢氧化钠反应生成硅酸钠和水,不能用陶瓷坩埚,故D错误;
故答案选A。

 阅读快车系列答案
阅读快车系列答案【题目】下图是牙膏中某些主要成分检验流程图,请回答以下问题:
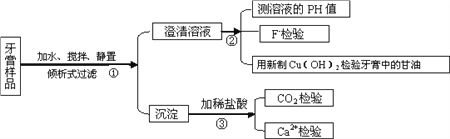
(1)牙膏中的摩擦剂约占牙膏成分的50%,主要用于增强牙膏的摩擦作用和去污效果,不同种类的牙膏含有的摩擦剂有所不同,在上述流程图的第③步加入盐酸后会产生不同现象,请你填空:
摩擦剂 | 实验中出现的现象 | 解 释 |
SiO2 | ________________ | _____________ |
CaCO3 | ________________ | ______________ |
Ca3(PO4)2 | 溶解无气体,加NaOH至过量后又产生沉淀 | ______________ |
Al(OH)3 | 溶解无气体,加NaOH至过量先产生沉淀后溶解 | _______________ |
(2)日常生活中使用的牙膏里面都含有一定量的摩擦剂,试回答下列相关问题:
A.根据你的推测,摩擦剂应具备下列性质中的哪几条?________________
①易溶于水 ②难溶于水 ③坚硬 ④柔软 ⑤颗粒较大 ⑥颗粒较小
B.据调查,两面针儿童牙膏、珍珠王防臭牙膏和中华透明牙膏中所使用的摩擦剂依次是氢氧化铝、碳酸钙和二氧化硅,它们所属的物质类别依次是________________、____________、___________。
C.作牙膏摩擦剂的粉末状碳酸钙可以用石灰石来制备。以下是一种制备碳酸钙的生产方案,其流程图为,请你写出上述方案中有关反应的化学方程式:
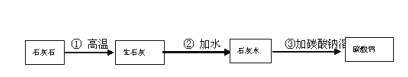
①_______________ ②________________ ③___________________
(3)新制Cu(OH)2的配制方法是__________________________。
牙膏中含有一定量的甘油,其主要功能是作保湿剂,在流程图的第②步得到的澄清溶液中加入新制Cu(OH)2,产生的现象是_____,化学方程式为_________
(4)实验测定澄清溶液的pH>7,可能原因是___________。
(5)牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:Ca5(PO4)3OH(固) ![]() 5Ca2++3PO43-+OH-
5Ca2++3PO43-+OH-
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是_____________________
已知Ca5(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因:_____________,根据以上原理,请你提出一种其它促进矿化的方法_________________________
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
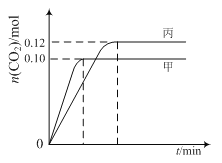
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)>v(逆)
D. T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
【题目】甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)甲醇脱氢可制取甲醛CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:

①600K时,Y点甲醇的υ(逆) (正)(填“>”或“<”)
②从Y点到X点可采取的措施是____________________________。
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判断:实验①的前20 min的平均反应速率 ν(H2)= ;实验温度T1 T2(填“>”、“<”);催化剂的催化效率:实验① 实验②(填“>”、“<”)。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程, 除去甲醇的离子方程式为 。

