题目内容
6.一定温度下,反应:N2(g)+3H2(g)?2NH3(g),达到化学平衡状态的标志是( )| A. | c(N2)﹕c(H2)﹕c(NH3)=1﹕3﹕2 | |
| B. | N2,H2和NH3的质量分数不再改变 | |
| C. | N2与H2的物质的量之和是NH3的物质的量的2倍 | |
| D. | 单位时间内每增加1mol N2,同时增加3mol H2 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,c(N2)﹕c(H2)﹕c(NH3)可能为1﹕3﹕2,也可能不是1﹕3﹕2,与各物质的初始浓度及转化率有关,故A错误;
B、N2,H2和NH3的质量分数不再改变,各物质的量不变,说明反应达平衡状态,故B正确;
C、平衡时反应物与生成物的物质的量关系取决于反应起始物质的量以及转化的程度,不能用来判断是否达到平衡状态,故C错误;
D、都表示的是逆反应速率,未体现正与逆的关系,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
16.清明假期期间各地对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图 ,下列关于该物质的说法正确的是( )
,下列关于该物质的说法正确的是( )
 ,下列关于该物质的说法正确的是( )
,下列关于该物质的说法正确的是( )| A. | 其分子式为C15H21O4 | |
| B. | 分子中只含有两种极性共价键 | |
| C. | 既能发生加聚反应,又能发生酯化反应 | |
| D. | 既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色 |
17.六种物质中,分别与盐酸、氢氧化钠溶液均能发生反应的是( )
①Al ②SiO2 ③A1(OH)3 ④NaHCO3 ⑤CH3COONH4 ⑥H2N-CH2-COOH.
①Al ②SiO2 ③A1(OH)3 ④NaHCO3 ⑤CH3COONH4 ⑥H2N-CH2-COOH.
| A. | 只有①③④ | B. | 只有②⑤⑥ | C. | 只有①③④⑥ | D. | 只有①③④⑤⑥ |
18.若溶液中由水电离产生的C (OH-)=1×10-14mol•L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A. | Al3+ Na+NO3- Cl- | B. | K+ Na+Cl- NO3- | ||
| C. | K+ Na+ Cl-AlO2- | D. | K+ NH4+ SO42-NO3- |
15.下列叙述正确的是( )
| A. | 固体时能导电的晶体一定为金属晶体 | |
| B. | 电负性差值小于1.7的A、B两种元素,组成的化合物也可能为离子化合物 | |
| C. | 某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体 | |
| D. | 由原子构成的晶体均具有熔沸点高、硬度大的特性 |
16.下列实验用来证明SO2的存在,其中正确的是( )
| A. | 不能使品红褪色 | |
| B. | 能使湿润的蓝色石蕊试纸变红 | |
| C. | 通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 | |
| D. | 通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸 |
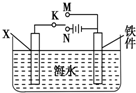 对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命. .
. ,B的结构简式
,B的结构简式 或
或 .
. ,反应类型:取代反应.
,反应类型:取代反应.