题目内容
18.已知第3周期某元素R的气态氢化物的化学式为H2R,下列叙述中不正确的是( )| A. | 该元素的原子最外电子层上有6个电子 | |
| B. | 该元素最高正价氧化物的化学式为RO2 | |
| C. | 该元素一定是非金属元素 | |
| D. | 该元素最高价氧化物的对应水化物的化学式为H2RO4 |
分析 第三周期元素R的气态氢化物的化学式为H2R,则R元素最低负化合价为-2,R为非金属元素,其最高正化合价为+6,R为S元素,结合化合价判断最外层电子数及相应化学式.
解答 解:第三周期元素R的气态氢化物的化学式为H2R,则R元素最低负化合价为-2,R为非金属元素,其最高正化合价为+6,R为S元素.
A.R元素最高正化合价为+6,故其原子最外层电子数为6,故A正确;
B.该元素的原子高正价为+6,则最高正化合价氧化物的化学式为SO3,故B错误;
C.由于元素R形成气态氢化物H2R,R元素最低负化合价为-2,R为非金属元素,故C正确;
D.该元素的原子高正价为+6,该元素最高价氧化物对应的水化物的化学式为H2SO4,故D正确,
故选B.
点评 本题考查原子结构与元素周期律,难度不大,注意根据元素化合价进行分析解答.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
8.在含有0.6molCl-、0.8molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.则( )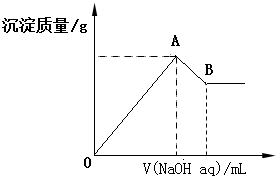

| A. | x=$\frac{2a}{5-a}$ | |
| B. | x的取值范围是0<x<$\frac{11}{32}$ | |
| C. | A点横坐标的值随x发生变化 | |
| D. | 若B点横坐标为200mL时,c(NaOH)=7.0mol/L |
9.在下列实验中,应将温度计插入水浴中的是( )
| A. | 在实验室中蒸馏石油 | B. | 由苯制硝基苯 | ||
| C. | 由酒精制乙烯 | D. | 由乙酸与乙醇反应制乙酸乙酯 |
6.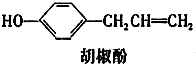 胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )
①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④该化合物与溴水反应,1mol最多可与2mol Br2发生反应.
 胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④该化合物与溴水反应,1mol最多可与2mol Br2发生反应.
| A. | ①③ | B. | ①②④ | C. | ②③ | D. | ②③④ |
13.下列说法正确的是( )
| A. | 化合物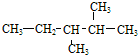 按系统命名法的名称为3,4-二甲基戊烷 按系统命名法的名称为3,4-二甲基戊烷 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 | |
| C. | 通常用酒精消毒,其原理是酒精使细菌中的蛋白质变性而失去生理活性 | |
| D. | 等质量的聚乙烯、甲烷、乙烯分别充分燃烧,所耗氧气的量依次减少 |
3.某气体中可能含NH3.HI.Cl2.CO2中一种或几种.将该气体通入硝酸银溶液产生黄色沉淀;将该气体通入澄清石灰水未观察到白色沉淀,则该气体( )
①一定含有HI ②一定不含CO2 ③可能含有CO2④一定不含NH3 ⑤一定不含Cl2.
①一定含有HI ②一定不含CO2 ③可能含有CO2④一定不含NH3 ⑤一定不含Cl2.
| A. | ①②④ | B. | ①②④⑤ | C. | ①③④⑤ | D. | ①②⑤ |
10.对于SO2和CO2的说法中正确的是( )
| A. | 都是直线形结构 | B. | 中心原子都采用SP杂化轨道 | ||
| C. | SO2为V形结构,CO2为直线形结构 | D. | S原子和C原子上都没有孤对电子 |
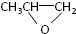 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物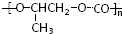 ,该反应符合绿化学的原则.
,该反应符合绿化学的原则.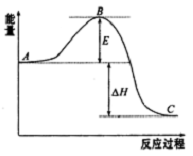 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1