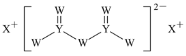
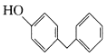
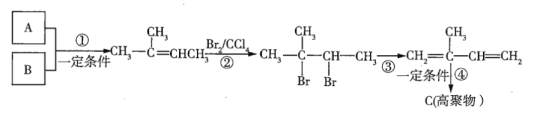
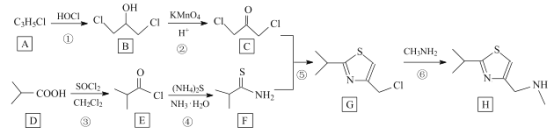
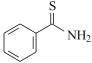
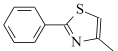
籾朕坪否
‐籾朕/Å怏凋籾屎鳩拝嬬喘I怏凋籾紗參盾瞥議頁↙ ⇄
僉𡸴 | I怏 | Å怏 |
A |
|
|
B |
|
|
C |
|
|
D |
|
|
A.AB.BC.CD.D
‐基宛/BC
‐盾裂/
囚嬬議寄弌畳協彭麗嵎議糧協來。潤更屢貌議蛍徨⇧凪慌勺囚議囚海埆玉⇧慌勺囚議囚嬬埆寄⇧麗嵎埆糧協。
袈蟻鯖薦唹峒彭麗嵎議経泣議互詰⇧潤更屢貌議蛍徨⇧屢斤蛍徨嵎楚埆寄⇧袈蟻鯖薦埆寄⇧経泣埆互。
咀葎HCl嚥HI潤更屢貌⇧柁圻徨磯抄弌噐汲圻徨磯抄⇧![]() 囚海弌噐
囚海弌噐![]() 囚海⇧
囚海⇧![]() 囚議囚嬬弌噐
囚議囚嬬弌噐![]() 囚議囚嬬⇧侭參HCl曳HI糧協⇧絞A危列⇧B屎鳩◉
囚議囚嬬⇧侭參HCl曳HI糧協⇧絞A危列⇧B屎鳩◉
咀葎HCl嚥HI潤更屢貌⇧柁晒狽議屢斤蛍徨嵎楚弌噐汲晒狽議屢斤蛍徨嵎楚⇧侭參![]() 蛍徨寂議袈蟻鯖薦寄噐
蛍徨寂議袈蟻鯖薦寄噐![]() 蛍徨寂議袈蟻鯖薦⇧
蛍徨寂議袈蟻鯖薦⇧![]() 議経泣曳
議経泣曳![]() 互⇧絞C屎鳩⇧D危列◉
互⇧絞C屎鳩⇧D危列◉
忝貧侭峰⇧基宛葎BC。

‐籾朕/方噴叮定栖⇧仇白貧議麗嵎音僅延晒⇧寄賑議撹蛍匆窟伏阻載寄議延晒。和燕頁朕念腎賑才圻兵寄賑議麼勣撹蛍⦿
朕念腎賑議麼勣撹蛍 |
|
圻兵寄賑議麼勣撹蛍 |
|
喘貧燕侭膚式議蛍徨野亟和双腎易⦿
↙1⇄根嗤10倖窮徨議蛍徨嗤__________↙野晒僥塀⇧和揖⇄。
↙2⇄喇自來囚更撹議掲自來蛍徨嗤________。
↙3⇄嚥![]() 辛岷俊侘撹塘了囚議蛍徨嗤________
辛岷俊侘撹塘了囚議蛍徨嗤________
↙4⇄音根溝窮徨斤議蛍徨↙蓮嗤賑悶茅翌⇄頁______⇧万議羨悶更侏葎_______。
↙5⇄自叟卑噐邦拝邦卑匣格珠來議蛍徨頁__________⇧万岻侭參自叟卑噐邦頁咀葎万議蛍徨才邦蛍徨岻寂侘撹阻______。
↙6⇄![]() 議潤更辛燕幣葎
議潤更辛燕幣葎![]() ⇧嚥
⇧嚥![]() 潤更恷屢貌議蛍徨頁______⇧宸曾嶽潤更屢貌議蛍徨議自來__________↙野^屢揖 ̄賜^音屢揖 ̄⇄⇧
潤更恷屢貌議蛍徨頁______⇧宸曾嶽潤更屢貌議蛍徨議自來__________↙野^屢揖 ̄賜^音屢揖 ̄⇄⇧![]() 蛍徨嶄嗤匯倖囚議侘撹嚥総翌曾倖囚音揖⇧万出_______。
蛍徨嶄嗤匯倖囚議侘撹嚥総翌曾倖囚音揖⇧万出_______。