题目内容
1.反应:4A(g)+5B(g)═4C(g)+6D(g)在不同条件下进行,用不同的物质表示其反应速率如下,则此反应在不同条件下进行最快的是( )| A. | v(A)=4 mol•L-1•min-1 | B. | v(B)=5 mol•L-1•min-1 | ||
| C. | v(C)=5 mol•L-1•min-1 | D. | v(D)=6 mol•L-1•min-1 |
分析 由于速率之比等于化学计量数之比,故不同物质表示化学反应速率与其化学计量数的比值越大,反应速率越快.
解答 解:由于速率之比等于化学计量数之比,故不同物质表示化学反应速率与其化学计量数的比值越大,反应速率越快,
A.$\frac{v(A)}{4}$=1 mol•L-1•min-1;
B.$\frac{v(B)}{5}$=1 mol•L-1•min-1;
C.$\frac{v(C)}{4}$=1.25 mol•L-1•min-1;
D.$\frac{v(D)}{6}$=1 mol•L-1•min-1,
故反应速率v(C)>v(A)=v(B)=v(D),
故选C.
点评 本题考查反应速率的比较,利用反应速率与化学计量数的比值可快速解答,也可转化为同种物质的反应速率来比较,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
11.根据下表部分短周期元素的原子半径及主要化合价信息回答以下问题:
(1)E与氢形成的化合物由两种分别是H2O、H2O2,其中心原子的杂化方式分别是sp3、sp3.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
16.下列各组物质,互为同分异构体的是( )
| A. | 氧气和臭氧 | B. | 乙烷和乙烯 | ||
| C. | 氕、氘和氚 | D. | 正戊烷、异戊烷和新戊烷 |
6.下列各组物质中,具有相同酸根的一组是( )
| A. | K2SO4、Na2SO3 | B. | K2MnO4、NaMnO4 | C. | CaCl2、NaCl | D. | NaCl、KClO3 |
13.下列反应物到生成物的转化不能直接实现的是( )
| A. | Ba(NO3)2─→BaSO4 | B. | H2SO4─→HCl | C. | CuO─→Cu(OH)2 | D. | Ba(OH)2─→Fe(OH)3 |
10.元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:硼元素的相对原子量为10.81.
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:
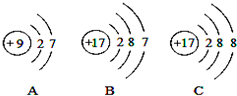
①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:

①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
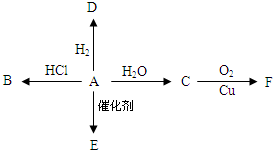 如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题
如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题