题目内容
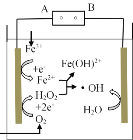
【题目】电-Fenton法是用于水体中有机污染物降解的高级氧化技术,反应原理如图所示。电解产生的H2O2与Fe2+发生反应生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法错误的是
A.电源的A极为负极
B.与电源B极相连电极的电极反应式为H2O-e- =H++·OH
C.Fenton反应为:H2O2+Fe2+=Fe(OH)2++·OH
D.每消耗2.24LO2(标准状况),整个电解池中理论上可产生的·OH为0.2mol
【答案】D
【解析】
根据图示,三价铁离子在左端电极得到电子转化为亚铁离子,发生还原反应,左端电极为阴极,则A为电源负极,B为电源正极,右端电极为阳极。
A. 根据上述分析,电源的A极为负极,故A正确;
B. 与电源B极相连电极为阳极,根据图示,水在阳极上失电子产生羟基自由基(·OH),电极反应式为H2O-e- =H++·OH,故B正确;
C. 电解产生的H2O2与Fe2+发生反应生成的羟基自由基(·OH),由图示装置可知,H2O-e- =H++·OH,Fe3++e-=Fe2+,O2+2e- +2H+=H2O2;则H2O2+Fe2+ =Fe(OH)2++·OH, Fenton反应为:H2O2+Fe2+=Fe(OH)2++·OH,故C正确;
D. D.每消耗1 mol O2,转移4 mol电子,根据H2O2+Fe2+ =Fe(OH)2+ +·OH反应看出转移1 mol电子,生成1mol·OH ,所以应当生成4 mol·OH,故D错误;
答案选D。

练习册系列答案
相关题目