题目内容
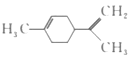
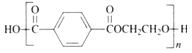
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,该材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

可采用的合成路线如图所示:
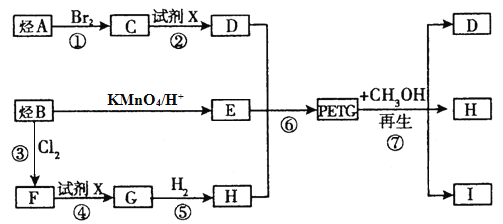
已知:①A的产量是衡量一个国家石油化工发展水平的重要标志之一。
②
![]()
③RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)C的名称为________,反应①的类型为_______。
(2)反应③所需条件为__________,试剂X为________。
(3)写出I的结构简式:___________。
(4)写出反应⑤的化学方程式:____________
(5)与E互为同分异构体,且满足以下条件的有机物共有_____种,其中核磁共振氢谱有4组峰,峰面积比为1:2:2:1的一种同分异构体的结构简式为_______。
①芳香化合物;②一定条件下能发生银镜反应;③能与NaHCO3溶液反应生成气体。
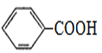
(6)请以甲苯为原料,设计制备苯甲酸苯甲酯的合成路线_____________。(无机试剂任选,合成路线示例见本题干)
【答案】1,2-二溴乙烷 加成反应 光照 NaOH溶液 ![]()
![]() +3H2
+3H2![]()
![]() 13
13 ![]()

【解析】
根据PETG的结构简式可以看出PETG是由![]() 、HOCH2CH2OH、
、HOCH2CH2OH、![]() 三种单体通过缩聚反应得到的一种高聚物;PETG和甲醇反应生成D、I和H,根据已知信息结合流程图可知D和H是醇,则E是
三种单体通过缩聚反应得到的一种高聚物;PETG和甲醇反应生成D、I和H,根据已知信息结合流程图可知D和H是醇,则E是![]() ,B和高锰酸钾反应生成E,则B是
,B和高锰酸钾反应生成E,则B是![]() ,B和氯气发生取代反应生成F为
,B和氯气发生取代反应生成F为![]() ,F发生水解反应生成G为
,F发生水解反应生成G为![]() ,G与氢气发生加成反应生成H是
,G与氢气发生加成反应生成H是![]() ,故D是乙二醇,则A是乙烯,乙烯和溴发生加成反应生成C为1,2-二溴乙烷,PETG和甲醇反应生成D、I和H,结合题给信息知,I是
,故D是乙二醇,则A是乙烯,乙烯和溴发生加成反应生成C为1,2-二溴乙烷,PETG和甲醇反应生成D、I和H,结合题给信息知,I是![]() ,据此解答。
,据此解答。
(1)C的结构简式为BrCH2CH2Br,名称为1,2-二溴乙烷。反应①是乙烯和溴的加成反应生成C。
(2)反应③是B和氯气的取代反应,所需条件为光照,F发生水解反应生成G,则试剂X为NaOH溶液。
(3)I的结构简式为![]() 。
。
(4)反应⑤是苯环和氢气的加成反应,反应的化学方程式为![]() +3H2
+3H2![]()
![]() 。
。
(5)与E(![]() )互为同分异构体,且满足以下条件①芳香化合物含有苯环;②一定条件下能发生银镜反应含有醛基;③能与NaHCO3溶液反应生成气体含有羧基。如果苯环上含有2个取代基,应该是-COOH和-OOCH,有邻间对三种;如果含有3个取代基,则应该是-COOH、-CHO和-OH,有10种,共计是13种。其中核磁共振氢谱有
)互为同分异构体,且满足以下条件①芳香化合物含有苯环;②一定条件下能发生银镜反应含有醛基;③能与NaHCO3溶液反应生成气体含有羧基。如果苯环上含有2个取代基,应该是-COOH和-OOCH,有邻间对三种;如果含有3个取代基,则应该是-COOH、-CHO和-OH,有10种,共计是13种。其中核磁共振氢谱有![]() 。
。
(6)根据已知信息结合逆推法可知以甲苯为原料制备苯甲酸苯甲酯的合成路线图为 。
。

【题目】利用碳和水蒸气制备水煤气的核心反应为:C(s)+H2O(g)H2(g)+CO(g)
(1)已知碳(石墨)、H2、CO的燃烧热分别为393.5kJ·mol-1、285.8kJ·mol-1、283kJ·mol-1,又知H2O(l)=H2O(g) ΔH=+44kJ·mol-1,则C(s)+H2O(g)CO(g)+H2(g) ΔH=___。
(2)在某温度下,在体积为1L的恒容密闭刚性容器中加入足量活性炭,并充入1mol H2O(g)发生上述反应,反应时间与容器内气体总压强的数据如表:
时间/min | 0 | 10 | 20 | 30 | 40 |
总压强/100kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
①平衡时,容器中气体总物质的量为________mol,H2O的转化率为________。
②该温度下反应的平衡分压常数Kp=________kPa(结果保留2位有效数字)。
(3)保持25℃、体积恒定的1L容器中投入足量活性炭和相关气体,发生可逆反应C+H2O(g)CO+H2并已建立平衡,在40 min时再充入一定量H2,50min时再次达到平衡,反应过程中各物质的浓度随时间变化如图所示:
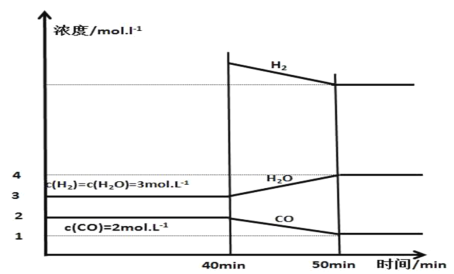
①40min时,再充入的H2的物质的量为________mol。
②40~50 min内H2的平均反应速率为________mol·L-1·min-1。
(4)新型的钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其原理如图所示:
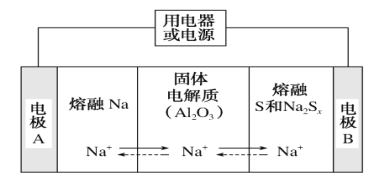
①放电时,电极A为________极,S发生________反应(填“氧化”或“还原”)。
②充电时,总反应为Na2Sx=2Na+Sx(3<x<5),Na所在电极与直流电源________极相连,阳极的电极反应式为_________。