ћвƒњƒЏ»Ё
°Њћвƒњ°њƒ≥–Ћ»§–°„йћљЊњ»№“Їµƒ pH ґ‘ KI ”л O2 Јі”¶µƒ”∞ѕм£ђ µ—й»зѕ¬°£
„∞÷√ | …’±≠÷–µƒ“Їће | ѕ÷ѕу |
| Ґў 2 mL 1 mol/L KI »№“Ї£Ђ5 µќµнЈџ | 5 Ј÷÷”Їуќё√чѕ‘±дїѓ |
ҐЏ 2 mL 1 mol/L KI »№“Ї£Ђ5 µќµнЈџ£Ђ2 mL 0.2 mol/L HCl »№“Ї | 5 Ј÷÷”Їу»№“Ї±дјґ | |
Ґџ 2 mL 1 mol/L KI »№“Ї£Ђ5 µќµнЈџ£Ђ2 mL 0.2 mol/L KCl »№“Ї | 5 Ј÷÷”Їуќё√чѕ‘±дїѓ | |
Ґ№ 2 mL pH£љ8.5 їм”– KOH µƒ 1 mol/L KI »№“Ї£Ђ5 µќµнЈџ | 5 –° ±Їу»№“Ї≤≈¬‘±дјґ | |
ҐЁ 2 mL pH£љ10їм”–KOHµƒ1 mol/L KI »№“Ї£Ђ5 µќµнЈџ | 5 –° ±Їуќё√чѕ‘±дїѓ |
(1) µ—饢÷–ќёѕ÷ѕу£ђњ…ƒ№µƒ‘≠“т «£Їi.KI”лO2≤їЈі”¶£ђii._____°£
(2)»фЈ≈÷√5–° ±Їу£ђ µ—饢÷–µƒ»№“Ї±дјґ£ђ‘тЈі”¶µƒјл„”Јљ≥ћ љ «_____°£
(3)»•µф µ—饟£ђґ‘Є√ћљЊњєэ≥ћ_____(ћо°∞”–°±їт°∞√ї”–°±)”∞ѕм°£
(4)ґ‘±» µ—饏ЇЌ µ—饹£ђњ…“‘µ√≥цµƒљб¬џ «_____°£
(5)ґ‘”Џ µ—饨µƒѕ÷ѕу£ђЉ„Ќђ—Іћб≥ц≤¬ѕл°∞pH=10 ±O2≤їƒ№—хїѓ I-°±£ђ…иЉ∆ЅЋѕ¬Ѕ–„∞÷√љш–– µ—饸£ђ—й÷§≤¬ѕл°£

i.…’±≠a ÷–µƒ»№“Їќ™_____°£
ii. µ—йљбєы «b ÷–»№“Ї±дјґ£ђіЋ≤¬ѕл≤ї≥…ЅҐ°£Ќ®»лO2Їу£ђa÷–µƒµзЉЂЈі”¶ љ «_____°£
iii. µ—饸µƒљбєыЋµ√ч µ—饨÷–°∞ќё√чѕ‘ѕ÷ѕуµƒ‘≠“т°± «_____°£
°Њір∞Є°њKI ”л O2 Јі”¶Ћў¬ ¬э 4I£≠+O2+2H2O=I2+4OH£≠ ”– KI ”л O2 Јі”¶‘ЏЋб–‘ћхЉюѕ¬Јі”¶Ћў¬ ±»Љо–‘ћхЉюѕ¬њм pH=10 µƒ KOH »№“Ї O2+2H2O+4e£≠= 4OH£≠ …ъ≥…µƒI2 ”л OH£≠Јі”¶
°Њљвќц°њ
(1) µ—饢÷–5 Ј÷÷”Їуќё√чѕ‘±дїѓњ…ƒ№ «Јі”¶≤Ґ√ї”–ЈҐ…ъ£ђ“≤њ…ƒ№ «Јі”¶Ћў¬ ћЂ¬э£ђ ±ЉдћЂґћ≤ї„г“‘єџ≤мµљѕ÷ѕу£ђ
є ір∞Єќ™£ЇKI ”лO2Јі”¶Ћў¬ ¬э£ї
(2)»фЈ≈÷√5–° ±Їу£ђ µ—饢÷–µƒ»№“Ї±дјґ£ђ «“тќ™µвјл„”ƒ№±ї—х∆ш—хїѓ≥…I2£ђЈі”¶јл„”Јљ≥ћ љќ™£Ї4I£≠+O2+2H2O=I2+4OH£≠£ї
є ір∞Єќ™£Ї4I£≠+O2+2H2O=I2+4OH£≠£ї
(3) ґ‘±» µ—饏ЇЌ µ—饟њ…“‘≈≈≥э¬»јл„”ґ‘Јі”¶µƒ”∞ѕм£ђ»зєы»•µф µ—饟‘т≤їƒ№Ћµ√ч¬»јл„”ґ‘Јі”¶ «Јс”–”∞ѕм£ђ
є ір∞Єќ™£Ї”–£ї
(4) ґ‘±» µ—饏ЇЌ µ—饹£ђ“їЄцЋб–‘ћхЉюѕ¬Јі”¶£ђ“їЄц «Љо–‘ћхЉюѕ¬Јі”¶£ђњ…“‘≈–ґѕ»№“ЇЋбЉо–‘ґ‘Јі”¶Ћў¬ µƒ”∞ѕм£ђ”…ѕ÷ѕуњ…÷™KI ”лO2Јі”¶‘ЏЋб–‘ћхЉюѕ¬Јі”¶Ћў¬ ±»Љо–‘ћхЉюѕ¬њм£ї
є ір∞Єќ™£ЇKI ”лO2Јі”¶‘ЏЋб–‘ћхЉюѕ¬Јі”¶Ћў¬ ±»Љо–‘ћхЉюѕ¬њм
(5)i£Ї“тЉ„Ќђ—Іћб≥ц≤¬ѕл°∞pH=10 ±O2≤їƒ№—хїѓI-°±£ђЋщ“‘Ќ®—х∆шµƒ“ї≤а…’±≠÷–”¶Љ”pH=10 µƒ KOH »№“Ї£ђ
є ір∞Єќ™: pH=10 µƒ KOH »№“Ї;
ii. µ—йљбєы «b ÷–»№“Ї±дјґ£ђЋµ√чpH=10 ±£ђ—х∆шњ…“‘—хїѓµвјл„”£ђі”ґшЋµ√ч≤¬ѕл≤ї≥…ЅҐ°£Ќ®»лO2Їу£ђa÷–µƒµзЉЂЈі”¶ љ «O2+2H2O+4e£≠= 4OH£≠£ђ
є ір∞Єќ™£ЇO2+2H2O+4e£≠= 4OH£≠£ї
iii. µ—饸µƒљбєыЋµ√чpH=10 ±£ђ—х∆шњ…“‘—хїѓµвјл„”£ђґш µ—饨÷–°∞ќё√чѕ‘ѕ÷ѕуµƒ‘≠“т°±÷їƒ№ «≤ъ…ъµƒµвµ•÷ ±їЉоѕыЇƒµЉ÷¬£ђЉі…ъ≥…µƒI2”л OH£≠Јі”¶£ђ
є ір∞Єќ™£Ї…ъ≥…µƒI2”л OH£≠Јі”¶£ї

 ‘ƒґЅњм≥µѕµЅ–ір∞Є
‘ƒґЅњм≥µѕµЅ–ір∞Є°Њћвƒњ°њѕ¬Ѕ– µ—йЈљ∞Є÷–ƒ№іпµљѕа”¶ µ—йƒњµƒµƒ «
A | B | C | D | |
Јљ∞Є |
|
|
»у ™µƒpH ‘÷љ |
љЂ NO2«тЈ÷±рљю≈Ё‘ЏјдЋЃЇЌ»»ЋЃ÷– |
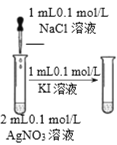
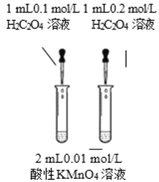
ƒњ µƒ | ÷§√чAgI ±»AgClЄьƒ—»№ | ћљЊњ≈®ґ»ґ‘їѓ—ІЈі”¶Ћў¬ µƒ”∞ѕм | ≤вґ®»№“Їµƒ pH | ћљЊњќ¬ґ»ґ‘їѓ—ІЈі”¶Ћў¬ µƒ”∞ѕм |
A.AB.BC.CD.D
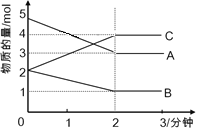
°Њћвƒњ°њ700 °ж ±£ђѕт»Ёїэќ™2 Lµƒ√№±’»Ё∆ч÷–≥д»л“їґ®ЅњµƒCOЇЌH2O£ђЈҐ…ъЈі”¶£ЇCO(g)£ЂH2O(g) CO2(g)£ЂH2(g)£ђЈі”¶єэ≥ћ÷–≤вґ®µƒ≤њЈ÷ эЊЁЉыѕ¬±н(±н÷–t2>t1)£Ї
Јі”¶ ±Љд/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.20 | |
t2 | 0.80 |
“јЊЁћв“вїЎірѕ¬Ѕ–ќ ћв£Ї
(1)Јі”¶‘Џt1 minƒЏµƒ∆љЊщЋў¬ ќ™v(H2)£љ________ mol°§L£≠1°§min£≠1°£
(2)±£≥÷∆дЋыћхЉю≤ї±д£ђ∆р Љ ±ѕт»Ё∆ч÷–≥д»л0.60 mol COЇЌ1.20 mol H2O£ђµљіп∆љЇв ±£ђn(CO2)£љ________mol°£
(3)ќ¬ґ»…э÷Ѕ800 °ж£ђ…ѕ цЈі”¶µƒ∆љЇв≥£ эќ™0.64£ђ‘т’эЈі”¶ќ™________Јі”¶(ћо°∞Ј≈»»°±їт°∞ќь»»°±)°£
(4)700 °ж ±£ђѕт»Ёїэќ™2 Lµƒ√№±’»Ё∆ч÷–≥д»лCO(g)°ҐH2O(g)°ҐCO2(g)°ҐH2(g)µƒќп÷ µƒЅњЈ÷±рќ™1.20 mol°Ґ2.00 mol°Ґ1.20 mol°Ґ1.20 mol£ђ‘тіЋ ±Є√Јі”¶v(’э)________v(ƒж)(ћо°∞>°±°∞<°±їт°∞£љ°±)°£
(5)Є√Јі”¶‘Џt1 ±њћіпµљ∆љЇв£ђ‘Џt2 ±њћ“тЄƒ±дƒ≥ЄцћхЉю£ђCOЇЌCO2≈®ґ»ЈҐ…ъ±дїѓµƒ«йњц»зЌЉЋщ Њ°£ЌЉ÷–t2 ±њћЈҐ…ъЄƒ±дµƒћхЉюњ…ƒ№ «________їт________°£
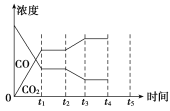
(6)»фЄ√»Ё∆ч»Ёїэ≤ї±д£ђƒ№Ћµ√чЈі”¶іпµљ∆љЇвµƒ «________°£
Ґўc(CO)”лc(H2)µƒ±»÷µ±£≥÷≤ї±д
ҐЏv(CO2)’э£љv(H2O)ƒж
Ґџћеѕµµƒ—є«њ≤ї‘ўЈҐ…ъ±дїѓ
Ґ№їмЇѕ∆шћеµƒ√№ґ»≤ї±д
ҐЁћеѕµµƒќ¬ґ»≤ї‘ўЈҐ…ъ±дїѓ
Ґё∆шћеµƒ∆љЊщѕаґ‘Ј÷„”÷ Ѕњ≤ї±д
°Њћвƒњ°њµзїѓ—І ÷ґќґ‘”Џ—–Њњќп÷ –‘÷ “‘Љ∞є§“µ…ъ≤ъ÷–ґЉ”–÷Ў“™Љџ÷µ°£
I. ƒ≥ µ—й–°„йјы”√‘≠µз≥Ў„∞÷√ґ‘ FeCl3”лNa2SO3µƒЈі”¶љш––ћљЊњ°£
„∞÷√ | µ—йѕ÷ѕу |
1 mol/L FeCl3»№“Ї(pH°÷1) 1mol/LNa2SO3 »№“Ї(pH°÷9) | Ѕй√фµзЅчЉ∆÷Є’лЈҐ…ъ∆Ђ„™ |
(1)»°…ўЅњ FeCl3»№“ЇµзЉЂЄљљьµƒїмЇѕ“Ї£ђЉ”»лћъ«иїѓЉЎ»№“Ї£ђ≤ъ…ъјґ…Ђ≥Ѕµн£ђ÷§√ч FeCl3„™їѓ≥…_____°£
(2)Љм—йЅн“їµзЉЂ≤ъќпµƒ≤ў„чЉ∞ѕ÷ѕу «_____°£
(3)ЄЇЉЂµƒµзЉЂЈі”¶ љќ™_____°£
II. є§“µ…ѕ”√ Na2SO4 »№“Їќь ’є§“µ—ћ∆ш÷–µƒµЌ≈®ґ» SO2 –ќ≥…ќь ’“ЇЇу£ђ‘ў≤…”√—фјл„”ƒ§µзљвЈ®£ђ њЎ÷∆µз—є£ђµзљвќь ’“Їњ…÷∆≥…≤ъ∆Ј S ЇЌ O2°£є§„ч‘≠јн Њ“вЌЉ»зѕ¬ЌЉ

“хЉЂ«шЇЌ—фЉЂ«шµƒpH Ћж ±Љдµƒ±дїѓєЎѕµ»зѕ¬ЌЉ£Ї

(4)—фЉЂЈі”¶µƒµзЉЂЈі”¶ќп « ____°£
(5)—фЉЂ«ш pH љµµЌµƒ‘≠“т «____°£(–і≥ц“їћхЉіњ…)
(6) љбЇѕµзЉЂЈі”¶ љ£ђЋµ√ч“хЉЂ«ш pH …эЄяµƒ‘≠“т_____°£(–і≥ц“їћхЉіњ…)