题目内容
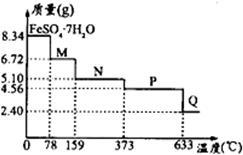
将8.34gFeSO4?7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示.则下列说法正确的是( )
| A.FeSO4?7H2O晶体中有4种不同结合力的水分子 | ||||
| B.在100℃时,M的化学式为FeSO4?6H2O | ||||
| C.在200℃时,N的化学式为FeSO4?3H2O | ||||
D.380℃的P加热至650℃时的化学方程式为:2FeSO4
|

8.34g FeS04?7H20样品物质的量=
=0.03mol,其中m(H20)=0.03mol×7×18g/mol=3.78g,如晶体全部失去结晶水,固体的质量应为8.34g-3.78g=4.56g,可知在加热到373℃之前,晶体失去部分结晶水,
A.温度为78℃时,固体质量为6.72g,其中m(FeS04)=0.03mol×152g/mol=4.56g,m(H20)=6.72g-4.56g=2.16g,n(H20)=
=0.12mol,则n(H20):n(FeS04)=0.12mol:0.03mol=4:1,则化学式为FeSO4?4H2O;温度为l59℃时,固体质量为5.10g,其中m(FeS04)=0.03mol×152g/mol=4.56g,m(H20)=5.10g-4.56g=0.54g,n(H20)=
=0.03mol,则n(H20):n(FeS04)=0.03mol:0.03mol=1:1,则化学式为FeSO4?H2O;加热至373℃时,固体的质量为4.56g,其中m(FeS04)=0.03mol×152g/mol=4.56g;加热至633℃时,固体的质量为2.40g,其中n(Fe)=n( FeS04?7H20)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,则固体中m(O)=2.40g-1.68g=0.72g,n(O)=
=0.045mol,则n(Fe):n(O)=0.03mol:0.045mol=2:3,则固体物质Q的化学式为Fe2O3,FeSO4?7H2O晶体中有3种不同B结合力的水分子,故A错误;
B、由A知在100℃时,M的化学式为FeSO4?4H2O和FeSO4?H2O的混合物,故B错误;
C、由A知在200℃时,N的化学式为FeSO4?3H2O和FeS04的混合物,故C错误;
D、由A知铁的化合价升高,必有硫的化合价降低,即有二氧化硫生成,设SO2、SO3的物质的量分别为x、y,则
解得
,所以方程式为:2FeSO4
Fe2O3+SO2↑+SO3↑,故D正确;
故选D.
| 8.34g |
| 278g/mol |
A.温度为78℃时,固体质量为6.72g,其中m(FeS04)=0.03mol×152g/mol=4.56g,m(H20)=6.72g-4.56g=2.16g,n(H20)=
| 2.16g |
| 18g/mol |
| 0.54g |
| 18g/mol |
| 0.72g |
| 16g/mol |
B、由A知在100℃时,M的化学式为FeSO4?4H2O和FeSO4?H2O的混合物,故B错误;
C、由A知在200℃时,N的化学式为FeSO4?3H2O和FeS04的混合物,故C错误;
D、由A知铁的化合价升高,必有硫的化合价降低,即有二氧化硫生成,设SO2、SO3的物质的量分别为x、y,则
|
解得
|
| ||
故选D.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目