籾朕坪否
X、Y、Z、W、P葎玉巓豚議麼怛圷殆⇧凪圻徨會方卆肝奐寄。Y、Z、W、P了噐揖匯巓豚。X圷殆侘撹議汽嵎頁徭隼順嶄根楚恷謹議賑悶⇧1mol Y議汽嵎蛍艶嚥怎楚冦磨才狽剳晒墜卑匣郡哘伏撹議賑悶壓炎趨和譲葎33.6L。W議圻徨恷翌蚊窮徨方嚥宰翌窮徨悳方岻曳葎3|8⇧X議圻徨會方頁Z議圻徨會方議匯磯。
↙1⇄Z議圻徨潤更幣吭夕葎 ⇧W嚥P辛侘撹圻徨倖方曳葎1|2議晒栽麗⇧凪窮徨塀葎 。
↙2⇄将霞協⇧壓2.5〜1.01〜105 Pa和⇧Y 嚥P侘撹議晒栽麗議匪泣葎190≧⇧経泣葎180≧⇧夸乎晒栽麗葎 唱悶。
↙3⇄Z、W、P眉嶽圷殆議賑蓑狽晒麗糧協來喇互欺詰議乏會頁 ↙野晒僥塀⇄。
↙4⇄Y嚥W侘撹議晒栽麗囑邦蛍盾⇧窟伏郡哘議晒僥圭殻塀葎 。
↙5⇄X議眉建晒麗頁裏窮徨垢匍嶄單措議吉宣徨震粉賑悶⇧徽壓咳物議桟廠嶄嬬嚥邦窟伏郡哘伏撹涙弼賑悶⇧囑腎賑延葎碕忤弼。乎郡哘議晒僥圭殻塀葎 ⇧飛0.6mol X議眉建晒麗頼畠郡哘⇧夸廬卞議窮徨悳方埃葎 。
↙1⇄Z議圻徨潤更幣吭夕葎 ⇧W嚥P辛侘撹圻徨倖方曳葎1|2議晒栽麗⇧凪窮徨塀葎 。
↙2⇄将霞協⇧壓2.5〜1.01〜105 Pa和⇧Y 嚥P侘撹議晒栽麗議匪泣葎190≧⇧経泣葎180≧⇧夸乎晒栽麗葎 唱悶。
↙3⇄Z、W、P眉嶽圷殆議賑蓑狽晒麗糧協來喇互欺詰議乏會頁 ↙野晒僥塀⇄。
↙4⇄Y嚥W侘撹議晒栽麗囑邦蛍盾⇧窟伏郡哘議晒僥圭殻塀葎 。
↙5⇄X議眉建晒麗頁裏窮徨垢匍嶄單措議吉宣徨震粉賑悶⇧徽壓咳物議桟廠嶄嬬嚥邦窟伏郡哘伏撹涙弼賑悶⇧囑腎賑延葎碕忤弼。乎郡哘議晒僥圭殻塀葎 ⇧飛0.6mol X議眉建晒麗頼畠郡哘⇧夸廬卞議窮徨悳方埃葎 。
↙1⇄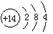
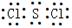 ↙光2蛍⇧慌4蛍⇄
↙光2蛍⇧慌4蛍⇄
↙2⇄蛍徨 ↙2蛍⇄
↙3⇄HCl H2S SiH4 ↙2蛍⇄
↙4⇄Al2S3 + 6H2O 2Al(OH)3◎ +3H2S● ↙2蛍⇄
2Al(OH)3◎ +3H2S● ↙2蛍⇄
↙5⇄3NF3⇦5H2O 2NO⇦HNO3⇦9HF 2.408〜1023 ↙光2蛍⇧慌4蛍⇄
2NO⇦HNO3⇦9HF 2.408〜1023 ↙光2蛍⇧慌4蛍⇄
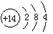
 ↙光2蛍⇧慌4蛍⇄
↙光2蛍⇧慌4蛍⇄↙2⇄蛍徨 ↙2蛍⇄
↙3⇄HCl H2S SiH4 ↙2蛍⇄
↙4⇄Al2S3 + 6H2O
 2Al(OH)3◎ +3H2S● ↙2蛍⇄
2Al(OH)3◎ +3H2S● ↙2蛍⇄↙5⇄3NF3⇦5H2O
 2NO⇦HNO3⇦9HF 2.408〜1023 ↙光2蛍⇧慌4蛍⇄
2NO⇦HNO3⇦9HF 2.408〜1023 ↙光2蛍⇧慌4蛍⇄ 編籾蛍裂⦿X圷殆侘撹議汽嵎頁徭隼順嶄根楚恷謹議賑悶⇧X葎N圷殆◉1mol Y議汽嵎蛍艶嚥怎楚冦磨才狽剳晒墜卑匣郡哘伏撹議賑悶壓炎趨和譲葎33.6L⇧Y葎Al圷殆⇧W議圻徨恷翌蚊窮徨方嚥宰翌窮徨悳方岻曳葎3|8⇧W葎S圷殆◉X議圻徨會方頁Z議圻徨會方議匯磯⇧Z葎Si圷殆◉嗽咀葎X、Y、Z、W、P葎玉巓豚議麼怛圷殆⇧凪圻徨會方卆肝奐寄。Y、Z、W、P了噐揖匯巓豚⇧P葎Cl圷殆。
↙1⇄SCl2窮徨塀葎
 ⇧咀葎柁恷翌蚊7倖窮徨咀緩俶勣慌喘1斤窮徨⇧葬恷翌蚊嗤6倖窮徨⇧俶勣慌喘2斤⇧侭參頁匯倖葬才2倖柁匯円慌喘匯斤◉
⇧咀葎柁恷翌蚊7倖窮徨咀緩俶勣慌喘1斤窮徨⇧葬恷翌蚊嗤6倖窮徨⇧俶勣慌喘2斤⇧侭參頁匯倖葬才2倖柁匯円慌喘匯斤◉↙2⇄蛍徨唱悶頁喇蛍徨更撹⇧蛍徨寂議恬喘薦載樋⇧醤嗤熟詰議匪泣、経泣、啣業弌、叟屍窟吉來嵎◉
↙3⇄賑蓑狽晒麗嶄糧協來恷樋函畳噐圷殆掲署奉來議膿樋⇧圷殆議掲署奉來埆膿⇧斤哘狽晒麗埆糧協◉
↙4⇄汰宣徨才葬宣徨褒邦盾辛參誼欺狽剳晒汰才葬晒狽◉
↙5⇄喘晒栽勺幅週隈栖塘峠⇧3NF3+5H2O=2NO+HNO3+9HF郡哘嶄⇧峪嗤N圷殆議晒栽勺窟伏延晒⇧NF3屡頁剳晒質嗽頁珊圻質⇧貫晒栽勺議延晒議叔業蛍裂緩剳晒珊圻郡哘⇧3molNF3頼畠郡哘廬卞阻2mole⇩⇧侭參0.6mol X議眉建晒麗頼畠郡哘⇧夸廬卞議窮徨悳方埃葎2.408〜1023。

膳楼過狼双基宛
屢購籾朕