题目内容
【题目】(题文)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。
(1)工业上的湿法制备方法是用KClO 与Fe(OH)3在KOH 存在下制得K2FeO4,该反应氧化剂与还原剂物质的量之比为_____________。
(2)实验室用食盐、废铁屑、硫酸、KOH等为原料,通过以下过程制备K2FeO4:
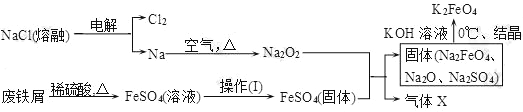
①操作(Ⅰ)的方法为在隔绝空气条件下________、________、过滤、洗涤、隔绝空气减压干燥。
②写出产生X气体的化学方程式_______________________________________。
(3)测定某K2FeO4样品的质量分数,实验步骤如下:
步骤1:准确称量1.0g样品,配制100mL溶液;
步骤2:准确量取25.00mL K2FeO4溶液加入到锥形瓶中;
步骤3:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-;
步骤4:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤5:加入二苯胺磺酸钠作指示剂,用0.1000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显紫红色),记下消耗(NH4)2Fe(SO4)溶液的体积,做3次平行实验,平均消耗30.00mL的(NH4)2Fe(SO4)2溶液。
已知:K2Cr2O7水溶液显黄色,滴定时发生的反应为:6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O。
①步骤2中准确量取25.00mLK2FeO4溶液加入到锥形瓶中所用的仪器是________。
②写出步骤3中发生反应的例子方程式___________________________________。
③根据上述实验数据,测定该样品中K2FeO4的质量分数为___________。(K2FeO4摩尔质量为198g/mol)。
【答案】3:2蒸发浓缩冷却结晶2Na2O2=2Na2O+O2酸式滴定管CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-79.2%
【解析】
(1)湿法制备高铁酸钾(K2FeO4),则FeO42-为产物,Fe(OH)3为反应物,化合价升高总共3价,由电子转移守恒可知,ClO-为反应物,Cl-为生成物,化合价降低共2将,化合价升降最小公倍数为6,故Fe(OH)3的系数为2,FeO42-的系数为2,ClO-的系数为3,Cl-的系数为3,根据电荷守恒可知,OH-为反应物,系数为4,由元素守恒可知H2O为生成物,其系数为5,离子方程式为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,该反应氧化剂与还原剂物质的量之比为3:2;(2)①操作(I)是溶液中得到硫酸亚铁晶体的方法为:蒸发浓缩、冷却结晶、过滤、洗涤、隔绝空气减压干燥;②过程分析可知X为氧气,根据流程可知由过氧化钠分解而得,反应的化学方程式为2Na2O2=2Na2O+O2;(3)①K2FeO4溶液具有强氧化性,准确量取25.00mL K2FeO4溶液加入到锥形瓶中应在酸式滴定管中量取;
②在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-,铬元素化合价+3价变化为+6价,铁元素+6价变化为+3价,结合电子守恒和电荷守恒配平得到离子方程式为:CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;③CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O,得到定量关系为:
2FeO42-~2CrO42-~Cr2O72-~6Fe2+,
2 6
n 0.0300L×0.1000mol/L
n=0.001mol,
100mL溶液中含有0.001mol×![]() =0.004mol,
=0.004mol,
测定该样品中K2FeO4的质量分数=![]() ×100%=79.2%。
×100%=79.2%。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案