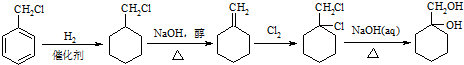
��Ŀ����
��֪����CH3CH2CH2NO2�����ȶ������Ȳ���NaOH��Һ��Ӧ���ֲ������ᷴӦ���ں��а���(��NH2)�Ļ�����ͨ���ܹ������ᷴӦ�����������Ρ��磺R��NH2+HCl��R��NH2��HCl(R��������)
��ͼ���л���M�����ģ�͵�ʾ��ͼ��
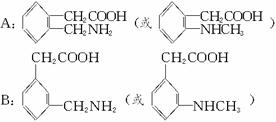
(1)��д��M�ķ���ʽ��________________________________��
(2)M��ͬ���칹���ж��֣�A��B��CΪ���е����֣��Ҷ��Ƿ����廯�����֪��
��A��B��C���ӵı����Ͼ�ֻ������ȡ��������ȡ����������ԭ���������l��
��A��B���������ᷴӦ�����ܱ�NaOH��Һ�кͣ������߱����ϵ�һȡ�����������ͬ��
��C�Ȳ���ǿ�ᷴӦ���ֲ���ǿ�Ӧ��
��д��A��B��C�Ľṹ��ʽ��
A__________________��B__________________��C__________________(C��д���е�һ��)��
(1)C9H11O2N
(2)




��ϰ��ϵ�д�
�����Ŀ


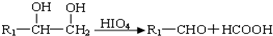

 ��W����Һ��ʹpH��ֽ��죬���ܷ���������Ӧ��
��W����Һ��ʹpH��ֽ��죬���ܷ���������Ӧ��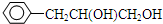

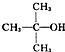 �ṹ���ƵĴ����ܱ�������ȩ���ᣮ�������͡�����ӣ������﹤�����й㷺��Ӧ��ǰ����PMAA����һ�֡������͡�����ӣ�������������ҩ�д������С���ӵķ��룮������������AΪ��ʼ��Ӧ��ϳɸ߷��ӻ�����PMAA��·�ߣ�
�ṹ���ƵĴ����ܱ�������ȩ���ᣮ�������͡�����ӣ������﹤�����й㷺��Ӧ��ǰ����PMAA����һ�֡������͡�����ӣ�������������ҩ�д������С���ӵķ��룮������������AΪ��ʼ��Ӧ��ϳɸ߷��ӻ�����PMAA��·�ߣ�

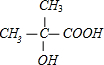
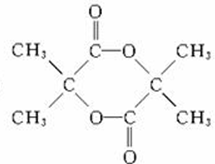
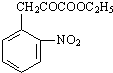 +H2O
+H2O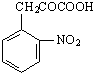 +C2H5OH
+C2H5OH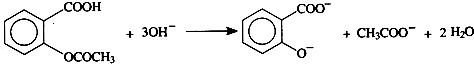
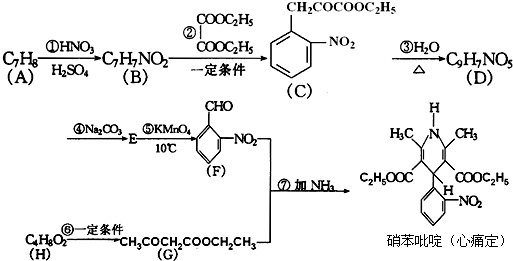
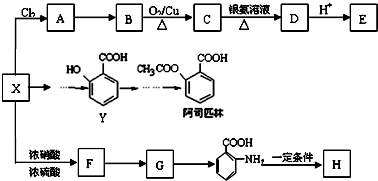 ij������X��һ����Ҫ���л�����ԭ�ϣ�������Է�������Ϊ92���о�������XΪ��ʼԭ����Ƴ�����ת����ϵͼ�����ֲ���ϳ�·�ߡ���Ӧ������ȥ��������A��һ�ȴ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO��
ij������X��һ����Ҫ���л�����ԭ�ϣ�������Է�������Ϊ92���о�������XΪ��ʼԭ����Ƴ�����ת����ϵͼ�����ֲ���ϳ�·�ߡ���Ӧ������ȥ��������A��һ�ȴ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO��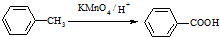
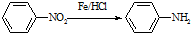 ���������ױ�������
���������ױ�������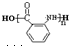
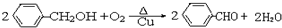

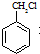 ����������ϳ�
����������ϳ�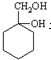 ���������ķ�����д���ϳ�·�ߣ���ע����Ӧ������
���������ķ�����д���ϳ�·�ߣ���ע����Ӧ������