题目内容
11.新制氯水中滴入下列溶液,不会发生反应的是( )| A. | 氯化钠 | B. | 硫酸亚铁 | C. | 硝酸银 | D. | KOH |
分析 氯气和水反应生成HCl、HClO,氯气和HClO具有强氧化性,HCl电离出氢离子而使氯水溶液呈酸性,据此分析解答.
解答 解:氯气和水反应生成HCl、HClO,氯气和HClO具有强氧化性,HCl电离出氢离子而使氯水溶液呈酸性,
A.氯化钠是强酸强碱盐,和氯气、HCl、HClO都不反应,故A选;
B.亚铁离子具有还原性,氯气和HClO具有强氧化性,所以二者发生氧化还原反应生成氯离子、铁离子,故B不选;
C.溶液中含有HCl,能和硝酸银溶液发生复分解反应生成AgCl沉淀,故C不选;
D.溶液中含有HCl、HClO,溶液呈酸性,能和KOH发生中和反应,故D不选;
故选A.
点评 本题以氯水为载体考查氧化还原反应、复分解反应,明确氯水成分及其性质是解本题关键,知道次氯酸的强氧化性和漂白性,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
2.下列表示物质的图或式正确的是( )
| A. | 氮气的电子式N┇┇N | B. | Mg2+的结构示意图 | ||
| C. | NH3的结构式 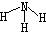 | D. | 甲基的电子式 |
19.下列物质中,属于纯净物的是( )
| A. | 白酒 | B. | 陈醋 | C. | 食用调和油 | D. | 蔗糖 |
6.下列关于原子的几种描述中,不正确的是( )
| A. | 18O与19F具有相同的中子数 | |
| B. | 16O与17O具有相同的电子数,互为同位素 | |
| C. | 15N与14N具有相同的质子数,是同种核素 | |
| D. | 12C与13C具有不同的质量数,属于同种元素 |
16.由下列实验事实得出的结论正确的是( )
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | 将SO2通入Ba(NO3)2溶液,有白色沉淀生成 | BaSO3难溶于硝酸 |
| C | Na2SiO3溶液中通CO2气体出现浑浊 | 酸性:H2SiO3<H2CO3 |
| D | 浓硫酸使蔗糖变黑 | 浓硫酸有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
3.下列各组离子在指定溶液中肯定大能量共存的是( )
| A. | 石蕊溶液呈蓝色的溶液:K+、Na+、NO3-、Cl- | |
| B. | 无色透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3- | |
| D. | 酸性溶液中:Al3+、Na+、SO42-、HCO3- |
20.铝制器皿能够盛放的物质是( )
| A. | 稀硝酸 | B. | 浓硫酸 | C. | NaOH溶液 | D. | 稀硫酸 |
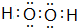 .固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-.
.固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-.