题目内容
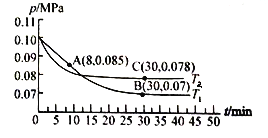
【题目】电导滴定是利用溶液的电导改变以确定滴定终点的滴定方法。常温下,将0.10mol·L-1CH2COOH溶液与0.10mo1·L-1HCl溶液以一定体积比混合,用0.10mol·L-1NaOH溶液滴定,滴定曲线如图所示。下列说法正确的是

A. a点溶液的pH=1
B. b点溶液中:c(Na+)=c(Clˉ)+c(CH3COOˉ)
C. 图中四点,C点处溶液中水的电离度最大
D. d点溶液中:c(Na+)>c(Clˉ)>c(CH3COOˉ)>c(OHˉ)>c(H+)
【答案】C
【解析】
A、等物质的量的盐酸和醋酸混合时,两者同时被稀释;
B、根据电荷守恒解析;
C、CH3COONa强碱弱酸盐,促进水电离;
D、图中V3-V2>V1,c(OHˉ)大于c(Clˉ)。
A、等物质的量的盐酸和醋酸混合时,两者同时被稀释,因醋酸是弱酸,只有部分电离,溶液中的氢离子浓度小于0.10mol·L-1,故溶液的pH大于1,故A错误;
B、b点溶液中的溶质为NaCl和CH3COOH,溶液显酸性,依据电荷守恒可知,c(Na+)<c(Clˉ)+c(CH3COOˉ),故B错误;
C、c点溶液中的溶质为NaCl和CH3COONa,醋酸根离子水解促进了水的电离,此时溶液中水的电离程度最大,故C正确;
D、d点溶液中的溶质为NaOH和CH3COONa,由图象可知,V3-V2>V1,故溶液中c(OHˉ)>c(Clˉ),故D错误;
故选C。

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案
相关题目