题目内容
6.下列离子方程式书写不正确的是( )| A. | 盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 少量CO2通入NaOH溶液中,:CO2+2OH-═CO32-+H2O | |
| C. | NaOH溶液和KHSO4溶液反应:OH-+H+═H2O | |
| D. | Na2O溶于稀盐酸:O2-+2H+═H2O |
分析 A.石灰石的主要成分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水;
B.二氧化碳少量,反应生成碳酸钠和水;
C.氢氧化钠与硫酸氢钠的反应实质为氢离子与氢氧根离子反应生成水;
D.氧化钠为氧化物,离子方程式中氧化钠不能拆开.
解答 解:A.盐酸滴在石灰石上,碳酸钙需要保留化学式,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故A正确;
B.少量CO2通入NaOH溶液中,反应生成碳酸钠和水,反应的离子方程式为:CO2+2OH-═CO32-+H2O,故B正确;
C.NaOH溶液和KHSO4溶液反应,硫酸氢钾完全电离,二者反应的离子方程式为:OH-+H+═H2O,故C正确;
D.氧化钠溶于稀盐酸,氧化钠应该保留化学式,正确的离子方程式为:Na2O+2H+═H2O+2Na+,故D错误;
故选D.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
16. 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )| A. | t1时刻之后,若再加入一定量的A,达平衡时A的转化率降低 | |
| B. | t1时刻之后,3v(A)逆=2v(C)正 (v-速率) | |
| C. | t1时刻之后,若升高温度,混合气体的平均摩尔质量增大,则该反应A消耗的方向为吸热反应 | |
| D. | 在温度和容积固定不变的条件下,起始投入1molB、3molC达平衡时A的体积分数为3/7 |
14.碘元素有“智力元素”之称.研究性学习小组做了如下实验探究海带中碘元素存在并测定其中碘元素的含量.
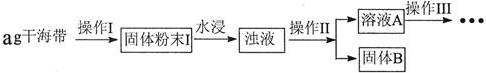
(1)操作Ⅰ为灼烧,则灼烧时用坩埚 盛装海带,操作Ⅱ为过滤
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性,I2+2S2O32-═2I-+S4O62-
将上述溶液稀释配制成200mL溶液,请完成下列实验探究.限选试剂:3%H2O2溶液、KSCN溶液、FeCL2溶液、稀硫酸
(4)定量检验海带中的碘含量:
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4
溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B
②在溶液B加入两滴淀粉溶液,用0.01mol/LNaS2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量$\frac{1.27V}{a}$×100%.
(假设操作Ⅰ、Ⅱ过程中碘不损失,原子量I-127)

(1)操作Ⅰ为灼烧,则灼烧时用坩埚 盛装海带,操作Ⅱ为过滤
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性,I2+2S2O32-═2I-+S4O62-
将上述溶液稀释配制成200mL溶液,请完成下列实验探究.限选试剂:3%H2O2溶液、KSCN溶液、FeCL2溶液、稀硫酸
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 |  |
| ② | 往试管Ⅰ中加入FeCl2溶液后,加入2滴KSCN溶液并振荡 | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4
溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B
②在溶液B加入两滴淀粉溶液,用0.01mol/LNaS2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量$\frac{1.27V}{a}$×100%.
(假设操作Ⅰ、Ⅱ过程中碘不损失,原子量I-127)
1.某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸进行中和热的测定.
Ⅰ.配制0.50mol•L-1 NaOH溶液
若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验.
(1)写出该反应的热化学方程式(中和热为57.3kJ•mol-1):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1
(2)取50mL NaOH溶液和30mL硫酸进行实验,实验数据如下表.
①请填写表中的空白:已知:反应后混合溶液的比热容c=4.2×10-3 kJ/(g•℃)
②用上述实验数值计算中和热-53.76kJ•mol-1(小数点后保留两位数字).
③能引起中和热偏高的原因是B
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
Ⅰ.配制0.50mol•L-1 NaOH溶液
若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验.
(1)写出该反应的热化学方程式(中和热为57.3kJ•mol-1):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1
(2)取50mL NaOH溶液和30mL硫酸进行实验,实验数据如下表.
①请填写表中的空白:已知:反应后混合溶液的比热容c=4.2×10-3 kJ/(g•℃)
| 温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0℃ |
| 2 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 3 | 26.4 | 26.2 | 26.3 | 30.4 | |
③能引起中和热偏高的原因是B
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
11.W、X、Y、Z是原子序数依次增大的四种短周期主族元素,W的阳离子能抑制水的电离,X、Z同主族,元素原子最外层电子数Z是Y的2倍,四种元素原子最外层电子数之和为16.下列说法正确的是( )
| A. | Y的最高价氧化物的水化物具有弱酸性 | |
| B. | 阳离子的氧化性:Y>W | |
| C. | 原子半径:Z>Y | |
| D. | 元素W、X、Z各自最高和最低化合价的代数和分别为0、4、4 |
18.等质量的N2和CO中,有可能不相等的是( )
| A. | 物质的量 | B. | 体积 | C. | 分子数 | D. | 原子数 |
 ).请用化学方程式表示其制备过程.
).请用化学方程式表示其制备过程.