题目内容
【题目】元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为_________________。
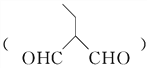
(2)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为_____
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示)_________
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是________________________________________
(5)C、N两元素形成的化合物C3N4形成的原子晶体,结构类似金刚石,甚至硬度超过金刚石,其原因是____________________________
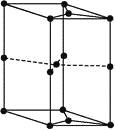
(6)如图为石墨晶胞结构示意图,该晶胞中含有碳原子的个数为______
【答案】1s22s22p63s23p63d64s2 5∶1 N>O>C HF分子间存在氢键,易形成缔合分子(HF)n 氮原子半径小于碳原子半径,氮碳形成的共价键键长比碳碳键键长短,键能更大,所以C3N4硬度更大 4
【解析】
(1)铁是26号元素,其核外电子排布式为1s22s22p63s23p63d64s2;
(2)C、H元素形成的化合物分子中共有16个电子的物质是CH2CH2,单键全是σ键,双键中有1个π键和1个σ键,故σ键与π键的个数比为5∶1;
(3)同一周期从左往右,第一电离能有逐渐增大趋势,且前四周期中ⅤA元素第一电离能比相邻元素大,故C、N、O三种元素的第一电离能由大到小的顺序为N>O>C;
(4)HF分子之间能形成氢键使分子缔合在一起,所以测得的相对分子质量为缔合分子的相对分子质量,故实验测得值一般高于理论值;
(5)原子晶体的硬度大小与共价键的强弱有关,共价键键长越短硬度越大,因氮原子半径小于碳原子半径,故C3N4晶体的硬度大于金刚石的硬度;
(6)顶点为8个晶胞所共有,棱上为4个晶胞所共有,面心为2个晶胞所共有,体内为晶胞所独有,石墨晶胞中含有碳原子的个数=![]() ×8+
×8+![]() ×4+
×4+![]() ×2+1×1=4。
×2+1×1=4。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案